题目内容
某研究小组欲检验草酸晶体样品分解产物并测定器质量分数(假设杂质不参与反应).草酸晶体( H2C2O4•2H2O)的理化性质见表.
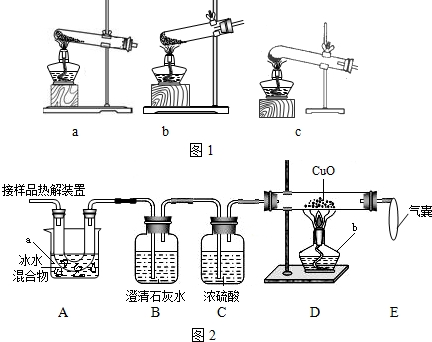
(1)加热分解草酸晶体最适宜的装置是 (填图1字母序号).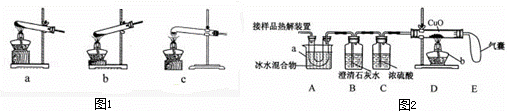
(2)图2是验证热分解产物中含CO,CO2的装置
①仪器a和b的名称分别是 和 .
②证明存在CO2的现象是 ,证明存在CO的现象是 ,D中反应的化学方程式是 .
③装置A的作用是 ,气囊的作用是 .
(3)为测定样品中草酸晶体的质量分数,设计两种如下方案.
| 熔点 | 沸点 | 热稳定性 | 与碱反应 |
| 101°C~102°C | 150°C~160°C升华 | 100.1°C失去结晶水,175°C分解成CO2,CO,H2O | 与Ca(OH)2反应产生白色沉淀(CaC2O4) |
①称一定量样品用上图装置进行实验,测得装置D反应前后的质量差,由此计算出的实验结果比实际值偏低,排除仪器和操作的因素,其原因可能有:CO未完全反应、 .
②称取8.75g草酸晶体样品配制50.00g溶液,取10.00g溶液加适量的稀硫酸,然后滴加25.00g3.16%KMnO4溶液,恰好反应完全.
(已知:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O)则KMnO4溶液显 色,25.00g3.16%KMnO4溶液中KMnO4的质量 g.请计算样品中的质量分数.[写出计算过程,M2(H2C2O4)=90,M2(H2C2O4•2H2O)=126,M2(KMnO4)=158].
| 草酸晶体的熔点较低,受热容易熔化; 要熟悉各种仪器的名称、用途; 书写化学方程式要注意规范性; 根据物质的性质可以进行相关方面的判断; 根据化学方程式可以计算草酸晶体的质量分数. | |
| 解答: | 解:(1)草酸的熔点较低,受热容易熔化,用c装置加热草酸时不容易下流,适宜用来加热草酸. 故填:c. (2)①仪器a和b的名称分别是烧杯、酒精灯. 故填:烧杯;酒精灯. ②证明存在CO2的现象是:B中澄清的石灰水变浑浊;证明存在CO的现象是:D中黑色固体变成红色. 故填:B中澄清的石灰水变浑浊;D中黑色固体变成红色. D中氧化铜和一氧化碳在加热时反应能生成铜和二氧化碳,反应的化学方程式是:CO+CuO 故填:CO+CuO ③装置A的作用是:除去草酸蒸汽,防止对二氧化碳的检验产生干扰;气囊的作用是:收集一氧化碳,防止污染空气. 故填:除去草酸蒸汽,防止对二氧化碳的检验产生干扰;收集一氧化碳,防止污染空气. (3)①一氧化碳部分反应,生成的铜重新被氧化等因素都能够导致计算出的实验结果比实际值偏低. 故填:生成的铜又被氧化. ②高锰酸钾溶液是颜色紫红色的. 故填:紫红. 25.00g3.16%KMnO4溶液中KMnO4的质量为:25.00g×3.16%=0.79g. 故填:0.79. 设10.00g溶液中含草酸晶体的质量为X, 由2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O可知, 5H2C2O4•2H2O→5H2C2O4→2KMnO4, 630 316 X 0.79g
X=1.575g, 50.00g溶液中含草酸晶体的质量为:1.575g×5=7.875g, 草酸晶体的质量分数为: 答:样品中草酸晶体的质量分数为90%. |

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案某研究小组欲检验草酸晶体样品分解产物并测定器质量分数(假设杂质不参与反应).草酸晶体(H2C2O4•2H2O)的理化性质见表.
(1)加热分解草酸晶体最适宜的装置是 (填图1字母序号).

(2)图2是验证热分解产物中含CO,CO2的装置
①仪器a和b的名称分别是 和 .
②证明存在CO2的现象是 ,证明存在CO的现象是 ,D中反应的化学方程式是 .
③装置A的作用是 ,气囊的作用是 .
(3)为测定样品中草酸晶体的质量分数,设计两种如下方案.
|
熔点 |
沸点 |
热稳定性 |
与碱反应 |
|
101°C~102°C |
150°C~160°C升华 |
100.1°C失去结晶水,175°C分解成CO2,CO,H2O |
与Ca(OH)2反应产生白色沉淀(CaC2O4) |
①称一定量样品用上图装置进行实验,测得装置D反应前后的质量差,由此计算出的实验结果比实际值偏低,排除仪器和操作的因素,其原因可能有:CO未完全反应、 .
②称取8.75g草酸晶体样品配制50.00g溶液,取10.00g溶液加适量的稀硫酸,然后滴加25.00g3.16%KMnO4溶液,恰好反应完全.
(已知:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O)则KMnO4溶液显 色,25.00g3.16%KMnO4溶液中KMnO4的质量 g.请计算样品中的质量分数.[写出计算过程,M2(H2C2O4)=90,M2(H2C2O4•2H2O)=126,M2(KMnO4)=158].
某研究小组欲检验草酸晶体样品分解产物,并测定样品中草酸晶体的质量分数(假设杂质不参与反应)。已知:浓硫酸可作为干燥剂;草酸晶体(H2C2O4·2H2O )的性质见下表:
|
熔点 |
沸点 |
热稳定性 |
其他 |
|
101℃~102℃ |
150℃~160℃升华 |
100.1℃分解出水,175℃分解成CO2、CO、H2O |
与 Ca(OH)2反应产生白色沉淀(CaC2O4) |
(1)图 1 是加热装置。最适宜的加热分解草酸晶体装置是C。若选装置 a 可能会造成的后果是_____________________;若选装置B可能会造成的后果是_________________。

(2)图 2 是验证热分解产物中含 CO 、 CO2的装置。

① 装置 A 的作用是_____________________,气囊的作用是_____________________。
② 证明存在 CO2的现象是______________,证明存在 CO 的现象是______________。
(3)为测定样品中草酸晶体的质量分数,设计如下方案:称取一定量样品,用上述装置进行实验,称量装置D反应前后的质量差。由此计算出的实验结果比实际值偏低,排除仪器和操作因素,其可能原因:_________________________________________________。
某研究小组欲检验草酸晶体样品分解产物并测定器质量分数(假设杂质不参与反应).草酸晶体( H2C2O4•2H2O)的理化性质见表.
(1)加热分解草酸晶体最适宜的装置是 (填图1字母序号).

(2)图2是验证热分解产物中含CO,CO2的装置
①仪器a和b的名称分别是 和 .
②证明存在CO2的现象是 ,证明存在CO的现象是 ,D中反应的化学方程式是 .
③装置A的作用是 ,气囊的作用是 .
(3)为测定样品中草酸晶体的质量分数,设计两种如下方案.
| 熔点 | 沸点 | 热稳定性 | 与碱反应 |
| 101°C~102°C | 150°C~160°C升华 | 100.1°C失去结晶水,175°C分解成CO2,CO,H2O | 与Ca(OH)2反应产生白色沉淀(CaC2O4) |
①称一定量样品用上图装置进行实验,测得装置D反应前后的质量差,由此计算出的实验结果比实际值偏低,排除仪器和操作的因素,其原因可能有:CO未完全反应、 .
②称取8.75g草酸晶体样品配制50.00g溶液,取10.00g溶液加适量的稀硫酸,然后滴加25.00g3.16%KMnO4溶液,恰好反应完全.
(已知:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O)则KMnO4溶液
显 色,25.00g3.16%KMnO4溶液中KMnO4的质量 g.请计算样品中的质量分数.[写出计算过程,M2(H2C2O4)=90,M2(H2C2O4•2H2O)=126,M2(KMnO4)=158].
某研究小组欲检验草酸晶体样品分解产物,并测定样品中草酸晶体的质量分数(假设杂质不参与反应)。已知:浓硫酸可作为干燥剂;草酸晶体(H2C2O4·2H2O )的性质见下表:
| 熔点 | 沸点 | 热稳定性 | 其他 |
| 101℃~102℃ | 150℃~160℃升华 | 100.1℃分解出水,175℃分解成CO2、CO、H2O | 与 Ca(OH)2反应产生白色沉淀(CaC2O4) |
(1)图 1 是加热装置。最适宜的加热分解草酸晶体装置是 c 。若选装置 a 可能会造成的后果是_____________________;若选装置 b 可能会造成的后果是_________________。

(2)图 2 是验证热分解产物中含 CO 、 CO2的装置。

① 装置 A 的作用是_____________________,气囊的作用是_____________________。
② 证明存在 CO2的现象是______________,证明存在 CO 的现象是______________。
(3)为测定样品中草酸晶体的质量分数,设计如下方案:称取一定量样品,用上述装置进行实验,称量装置 D 反应前后的质量差。由此计算出的实验结果比实际值偏低,排除仪器和操作因素,其可能原因:_________________________________________________。
 Cu+CO2.
Cu+CO2.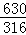 =
=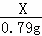
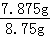 ×100%=90%,
×100%=90%,