题目内容
某研究小组欲检验草酸晶体样品分解产物并测定器质量分数(假设杂质不参与反应).草酸晶体( H2C2O4•2H2O)的理化性质见表.
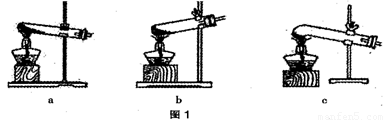
(1)加热分解草酸晶体最适宜的装置是 (填图1字母序号).

(2)图2是验证热分解产物中含CO,CO2的装置
①仪器a和b的名称分别是 和 .
②证明存在CO2的现象是 ,证明存在CO的现象是 ,D中反应的化学方程式是 .
③装置A的作用是 ,气囊的作用是 .
(3)为测定样品中草酸晶体的质量分数,设计两种如下方案.
| 熔点 | 沸点 | 热稳定性 | 与碱反应 |
| 101°C~102°C | 150°C~160°C升华 | 100.1°C失去结晶水,175°C分解成CO2,CO,H2O | 与Ca(OH)2反应产生白色沉淀(CaC2O4) |
①称一定量样品用上图装置进行实验,测得装置D反应前后的质量差,由此计算出的实验结果比实际值偏低,排除仪器和操作的因素,其原因可能有:CO未完全反应、 .
②称取8.75g草酸晶体样品配制50.00g溶液,取10.00g溶液加适量的稀硫酸,然后滴加25.00g3.16%KMnO4溶液,恰好反应完全.
(已知:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O)则KMnO4溶液
显 色,25.00g3.16%KMnO4溶液中KMnO4的质量 g.请计算样品中的质量分数.[写出计算过程,M2(H2C2O4)=90,M2(H2C2O4•2H2O)=126,M2(KMnO4)=158].
(1) c ①烧杯 酒精灯 ② B中澄清的石灰水变浑浊 D中黑色固体变成红色
CO+CuO Cu+CO2
Cu+CO2
③ 除去草酸蒸汽,防止对二氧化碳的检验产生干扰 收集一氧化碳,防止污染空气
(3)① 生成的铜又被氧化 ②紫红 0.79
设10.00g溶液中含草酸晶体的质量为X,
由2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O可知,
5H2C2O4•2H2O→5H2C2O4→2KMnO4, 630 316
X 0.79g
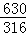 =
=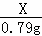
X=1.575g,
50.00g溶液中含草酸晶体的质量为:1.575g×5=7.875g,
草酸晶体的质量分数为: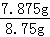 ×100%=90%,
×100%=90%,
答:样品中草酸晶体的质量分数为90%.

某研究小组欲检验草酸晶体样品分解产物并测定器质量分数(假设杂质不参与反应).草酸晶体(H2C2O4•2H2O)的理化性质见表.
(1)加热分解草酸晶体最适宜的装置是 (填图1字母序号).
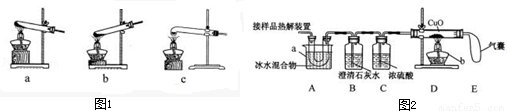
(2)图2是验证热分解产物中含CO,CO2的装置
①仪器a和b的名称分别是 和 .
②证明存在CO2的现象是 ,证明存在CO的现象是 ,D中反应的化学方程式是 .
③装置A的作用是 ,气囊的作用是 .
(3)为测定样品中草酸晶体的质量分数,设计两种如下方案.
|
熔点 |
沸点 |
热稳定性 |
与碱反应 |
|
101°C~102°C |
150°C~160°C升华 |
100.1°C失去结晶水,175°C分解成CO2,CO,H2O |
与Ca(OH)2反应产生白色沉淀(CaC2O4) |
①称一定量样品用上图装置进行实验,测得装置D反应前后的质量差,由此计算出的实验结果比实际值偏低,排除仪器和操作的因素,其原因可能有:CO未完全反应、 .
②称取8.75g草酸晶体样品配制50.00g溶液,取10.00g溶液加适量的稀硫酸,然后滴加25.00g3.16%KMnO4溶液,恰好反应完全.
(已知:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O)则KMnO4溶液显 色,25.00g3.16%KMnO4溶液中KMnO4的质量 g.请计算样品中的质量分数.[写出计算过程,M2(H2C2O4)=90,M2(H2C2O4•2H2O)=126,M2(KMnO4)=158].
某研究小组欲检验草酸晶体样品分解产物,并测定样品中草酸晶体的质量分数(假设杂质不参与反应)。已知:浓硫酸可作为干燥剂;草酸晶体(H2C2O4·2H2O )的性质见下表:
|
熔点 |
沸点 |
热稳定性 |
其他 |
|
101℃~102℃ |
150℃~160℃升华 |
100.1℃分解出水,175℃分解成CO2、CO、H2O |
与 Ca(OH)2反应产生白色沉淀(CaC2O4) |
(1)图 1 是加热装置。最适宜的加热分解草酸晶体装置是C。若选装置 a 可能会造成的后果是_____________________;若选装置B可能会造成的后果是_________________。
(2)图 2 是验证热分解产物中含 CO 、 CO2的装置。
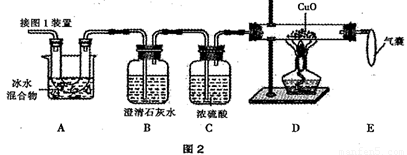
① 装置 A 的作用是_____________________,气囊的作用是_____________________。
② 证明存在 CO2的现象是______________,证明存在 CO 的现象是______________。
(3)为测定样品中草酸晶体的质量分数,设计如下方案:称取一定量样品,用上述装置进行实验,称量装置D反应前后的质量差。由此计算出的实验结果比实际值偏低,排除仪器和操作因素,其可能原因:_________________________________________________。
某研究小组欲检验草酸晶体样品分解产物,并测定样品中草酸晶体的质量分数(假设杂质不参与反应)。已知:浓硫酸可作为干燥剂;草酸晶体(H2C2O4·2H2O )的性质见下表:
| 熔点 | 沸点 | 热稳定性 | 其他 |
| 101℃~102℃ | 150℃~160℃升华 | 100.1℃分解出水,175℃分解成CO2、CO、H2O | 与 Ca(OH)2反应产生白色沉淀(CaC2O4) |
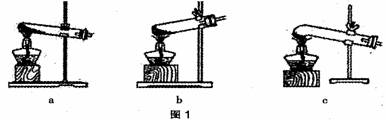
(1)图 1 是加热装置。最适宜的加热分解草酸晶体装置是 c 。若选装置 a 可能会造成的后果是_____________________;若选装置 b 可能会造成的后果是_________________。
(2)图 2 是验证热分解产物中含 CO 、 CO2的装置。

① 装置 A 的作用是_____________________,气囊的作用是_____________________。
② 证明存在 CO2的现象是______________,证明存在 CO 的现象是______________。
(3)为测定样品中草酸晶体的质量分数,设计如下方案:称取一定量样品,用上述装置进行实验,称量装置 D 反应前后的质量差。由此计算出的实验结果比实际值偏低,排除仪器和操作因素,其可能原因:_________________________________________________。
