题目内容
【题目】47中化学兴趣小组的同学为测定氯化钠和碳酸钠混合物的组成情况,某研究小组进行了如下实验。
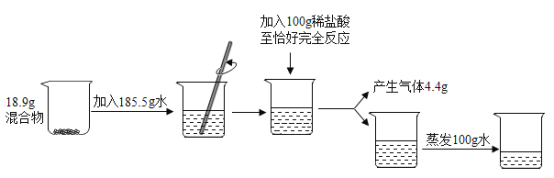
(1)实验中发生反应的化学方程式为_____。
(2)求解混合物中发生反应物质的质量(x)的比例式为_____。
(3)混合物中氯化钠和碳酸钠质量的最简整数比为_____。
(4)蒸发后所得溶液的溶质质量分数为_____。
(5)若用36.5%的浓盐酸配制实验所用的稀盐酸需加水的质量_____。
(6)若将实验后的溶液进行蒸发,得到氯化钠固体所需要的仪器有酒精灯、蒸发皿,还需要的仪器有_____。
【答案】(1)![]()
(2)![]()
(3)83:106
(4)10%
(5)80g
(6)(带铁圈的)铁架台、玻璃棒
【解析】
(1)稀盐酸和碳酸钠反应生成氯化钠二氧化碳和水,化学方程式为![]() ,故填:
,故填:![]() 。
。
(2)由反应流程图可知生成的气体为二氧化碳质量为4.4g设,发生反应碳酸钠质量为x生成的氯化钠质量为y,反应氯化氢质量为z。
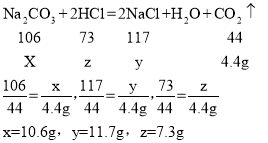
故填:![]()
(3)由比例关系![]() ,X=10.6g,故氯化钠质量;18.9g-10.6g=8.3g,
,X=10.6g,故氯化钠质量;18.9g-10.6g=8.3g,
故混合物中氯化钠和碳酸钠质量的最简整数比为:83:106,故填:83:106。
(4)蒸发后所得溶液的溶质质量为:8.3g+11.7g=20g,
蒸发后溶液质量;18.9g+185.5g+100g-4.4g-100g=200g,
故溶质质量分数:
![]()
故填:10%。
(5)配制100g稀盐酸所需36.5%的浓盐酸的质量设为m,根据稀释前后溶质质量不变;
m×36.5%=7.3g,m=20g,水的质量为;100g-20g=80g,故需要加水80g。
(6)若将实验后的溶液进行蒸发,得到氯化钠固体所需要的仪器有酒精灯、蒸发皿,还需要的仪器有(带铁圈的)铁架台、玻璃棒,故填:(带铁圈的)铁架台、玻璃棒。

【题目】分类和类比是学习化学常用方法。
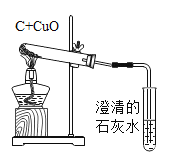
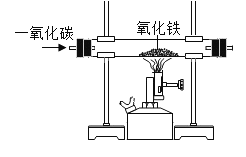
(1)化学是一门以实验为基础的科学,下面是我们在初中化学课本经历的实验:
|
|
|
|
A | B | C | D |
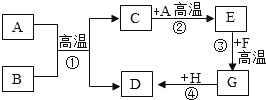
根据化学方程式提供的信息将上述实验平均分两类,选出的一组实验是_____。你的分类依据是_____。
(2)已知H2、CO、C是初中常见的还原剂,请根据它们还原氧化铜的方程式中各元素化合价的变化情况,分析在反应![]() 中作为还原剂的是_____,该反应的氧化剂中发生改变的元素,其化合价的变化情况是_____。
中作为还原剂的是_____,该反应的氧化剂中发生改变的元素,其化合价的变化情况是_____。
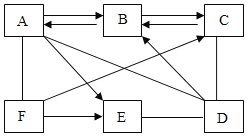
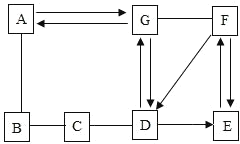
【题目】下图中直线相连物质间在一定条件下可以发生反应。下表提供的四组物质符合图中要求的是( )
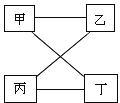
甲 | 乙 | 丙 | 丁 | |
A | Ca(OH)2 | CO2 | NaOH | CuSO4 |
B | Na2CO3 | BaCl2 | HCl | Ca(OH)2 |
C | Zn | HCl | CuCl2 | NaOH |
D | H2 | O2 | HCl | CuO |
A.AB.BC.CD.D