题目内容
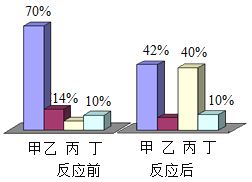
【题目】在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下反应,测得反应前后各物质的质量分数如图所示。下列说法正确的是( )
A.丙可能是单质
B.若消耗 3 g 的乙,则生成 17 g 的丙
C.丁一定是该反应的催化剂
D.甲、乙的质量之和一定等于生成丙的质量
【答案】B
【解析】
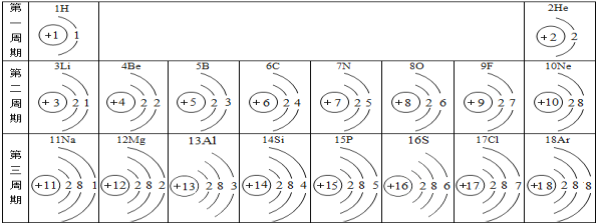
由四种物质反应前后各物质的质量分数可知,反应前后甲的质量分数减少了70%-42%=28%,故甲是反应物;同理可以确定乙的质量分数减少了14%-(1-42%-40%-10%)=6%,故乙是反应物;丙的质量分数增加了40%-(1-70%-14%-10%)=34%,丙是生成物;丁的质量分数不变,可能作该反应的催化剂,也可能没有参加反应。
A、该反应的反应物为甲和乙,生成物是丙,符合“多变一”的特征,属于化合反应,丙一定是化合物,故选项说法错误;
B、参加反应的乙和生成的丙的质量比为6%:34%=3:17,则若消耗3g的乙,则生成17g的丙,故选项说法正确;
C、丁的质量分数不变,可能作该反应的催化剂,也可能没有参加反应,故选项说法错误;
D、该反应的反应物为甲和乙,生成物是丙,根据质量守恒定律,参加反应的甲、乙的质量之和(而不是甲、乙的质量之和)一定等于生成丙的质量,故选项说法错误。
故选B。

 阅读快车系列答案
阅读快车系列答案【题目】实验室制取气体。
实验一组:研究氧气的制取
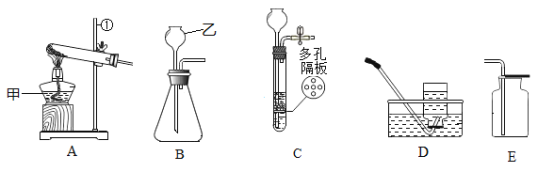
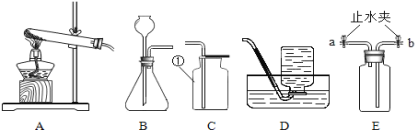
(1)写出仪器乙的名称_____。
(2)在实验室中,某同学选择高锰酸钾制取氧气,反应的化学方程式为_____。用A装置进行实验时,需要进行的改进是_____。
实验二组:研究二氧化碳的制取
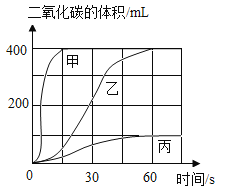
(3)选用药品。按下表进行实验,取等质量的大理石加入足量酸中(杂质不与酸反应),产生二氧化碳的体积随时间变化曲线如下图所示
实验编号 | 药品 |
Ⅰ | 块状大理石、10%稀硫酸(H2SO4) |
Ⅱ | 块状大理石、7%稀盐酸 |
Ⅲ | 大理石粉末、7%稀盐酸 |
上表中实验Ⅰ对应如图曲线_____(选填“甲”、“乙”或“丙”)。小组同学决定用实验Ⅱ的药品制取二氧化碳气体,不用实验Ⅲ药品制备二氧化碳的原因是_____。
(4)选择装置。实验小组同学制取二氧化碳时想要控制反应的开始和结束,应选择的发生装置为_____,用下图E装置收集二氧化碳时,验满的操作是_____。
(5)性质实验。某兴趣小组的同学利用下图装置研究二氧化碳的性质。(仪器的固定装置已经省略)
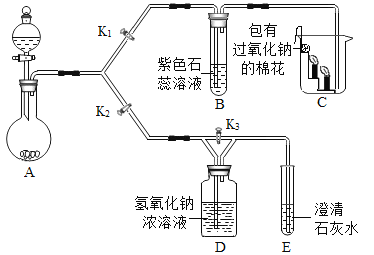
①A装置用于实验室制取二氧化碳。
②实验开始后,关闭K2、打开K1,可观察到B中现象为_____;C中的蜡烛由下至上依次熄灭,说明二氧化碳具有的性质是_____;
③实验开始后,关闭K1,打开K2和K3,写出E中发生反应的化学方程式_____。