��Ŀ����
����Ŀ��ͬѧ���ڰ���ʦ����ʵ����ʱ������ʯ��ˮ�Լ�ƿƿ�ں�ƿ����Χ��һЩ��ɫ��ĩ��Ϊ��Ū�����ɫ��ĩ�ijɷּ��γ�ԭ�����ǽ���������̽����
�����ϣ������Ǽ������ʳ���ʱ���ܼ�����
����̪�Լ���������Һ���ɫ��ʯ��ˮ��Һ�Լ���
OH�� | Cl�� | CO32�� | NO3�� | |
Ca2+ | | �� | �� | �� |
��1����ɫ��ĩ�ɷֵIJ���ͳ���
��ɫ��ĩ�ijɷ� | �γɵ�ԭ�� |
������CaCO3 | ��Ӧ�Ļ�ѧ����ʽΪ��_____ |
������Ca��OH��2 | ������½ϸߣ����ʵ��ܽ�Ƚ��ͻ��ܼ�������ʯ��ˮ�е����ʽᾧ���� |
��������˼����ͬѧ����Ϊ��ɫ��ĩ�������Ƕ��ߵĻ���
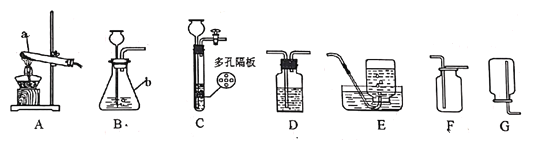
��2�����ʵ�飺��ͬѧȡ��ɫ��ĩװ���Թ��У���������ˮ�������а�ɫ���岻�ܽ⣬�������ó���ĩ��һ����CaCO3��������Ϊ��ͬѧ�Ľ��۲����ܣ�������_____��Ϊ�˵ó������ܵĽ��ۣ����ǽ���������ʵ�飬���������ʵ�鱨�棺
ʵ�鲽�� | ���ܹ۲쵽������ | ���� |
ȡ�����Թ��е��ϴ���ҹ���μ�1��2����ɫ��̪��Һ | _____ | _____ |
�������Թ��еIJ��������м���ϡ���� | _____ | ��ɫ��ĩ_____�����С����ޡ���CaCO3 |
������ʵ���֪��ɫ��ĩ�ijɷ��ǣ�_____�� | ||
��3��ʵ��Ӧ�ã���ʢ��̼��Ʒ�ĩ���Թ��м���������ϡ���ᣬ��ȫ��Ӧ���ռ���4.4g������̼���壬�Լ��㷴Ӧ���ĵ�̼��Ƶ�����_____��
���𰸡�CO2+Ca��OH��2��CaCO3��+H2O Ca��OH��2����ˮ����������������ƣ� ��̪��Һ���ɫ ��ɫ��ĩ����Ca��OH��2 �����ܽ⣬�����ݲ��� �� CaCO3��Ca��OH��2�Ļ���� 10g
��������
��1������ɫ����Ϊ̼��ƣ���Ӧ�����������ƺͶ�����̼��Ӧ�����ɵģ��ʿ���д���÷�Ӧ�Ļ�ѧ����ʽCO2+Ca��OH��2��CaCO3��+H2O��
��2�������ܽ�ȱ���֪��̼��Ʋ�����ˮ����������������ˮ�����Լ�ͬѧ�Ľ��۲���ȷ��Ҫ��֤�ð�ɫ�������ɿ��Խ���������ƺ�̼��Ƶ�������ѡ���̪��Һ�����������飻
ʵ�鲽�� | ���ܹ۲쵽������ | ���� |
��̪��Һ���ɫ | ��ɫ��ĩ����Ca��OH��2 | |
�����ܽ⣬�����ݲ��� | �� | |
CaCO3��Ca��OH��2�Ļ���� | ||
��3����Ӧ���ĵ�̼��Ƶ�����Ϊx
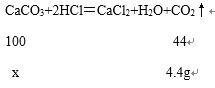
![]()
x��10g

 �����Ļ�������ҵϵ�д�
�����Ļ�������ҵϵ�д�����Ŀ��ij��ѧС��ͬѧ�������������ͭ����ʵ��Ĺ����У����������벻������������Һ��Ϊ����ɫ�� Ϊ̽����Һ���̵�ԭ����ϵ��ʵ�顣
���������ϣ�������ͭ��CuO��Ϊ��ɫ������ͭ���ӣ�Cu2+����ˮ��Һ�г���ɫ
������ʵ�飩
ʵ�� 1��ȡ 2mL ��ͬŨ�ȵ�����ֱ���뵽ʢ�� 0.2g ����ͭ���Թ��У�����ʵ�顣
��� | Ũ������ˮ�� ����� | ���� |
1-1 | 1:1 | 30 �����Һ��Ϊ��ɫ����ɫ����ʣ�� |
1-2 | 1:2 | 1 ���Ӻ���Һ��Ϊ����ɫ�� ��ɫ����ʣ�� |
1-3 | 1:3 | 2 ���Ӻ���Һ��Ϊ��ɫ����ɫ����ʣ�� |
1-4 | 1:4 | 4 ���Ӻ���Һ��Ϊdz��ɫ���к�ɫ����ʣ���Ҳ��ټ��� |
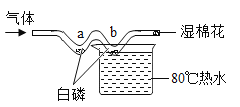
ʵ�� 2��ȡ 2mL ϡ���ᣨŨ������ˮ�������Ϊ 1:3�����뵽ʢ�� 0.2g ����ͭ���Թ��У�ʵ��װ�����¡�
��� | 2-1 | 2-2 |
���� |
|
|
���� | 2 ���Ӻ���Һ��Ϊ��ɫ���� �����ɫ����ʣ�� | 10 �����Һ��Ϊdz��ɫ���� ��ɫ����ʣ�� |
����������ۣ�
��1����ȫ����ͭ�����ᷴӦ�Ļ�ѧ����ʽ��CuO+2HCl ==== CuCl2+_________________
��2��ʵ�� 1 �����Ʋ�ͬŨ�ȵ�����ʱ����Ҫʹ�õ���������______________________������ţ���ͬ����
A ��Ͳ B �ձ� C �ƾ��� D ������
��3��ʵ�� 1 ��Ŀ����_______________��
��4�����ʵ�� 1 ��ʵ�� 2���ó��Ľ�����______________________��
����˼�����ۣ�
��span>5��ʵ�� 1-4 �У����к�ɫ����ʣ������ԭ����___________________��
��6��ʵ�� 1 ��������Ũ������ˮ�������Ϊ 1:5 ��ʵ�飬��ַ�Ӧ����ܳ��ֵ�����Ϊ ______________��
A ��Һ��Ϊ��ɫ����ɫ����ʣ��
B ��Һ��Ϊ��dz����ɫ����ɫ����ʣ�� C����Һ��Ϊ��dz����ɫ���к�ɫ����ʣ��