题目内容
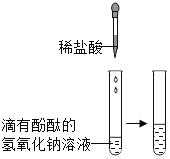
【题目】某化学兴趣小组的同学向氢氧化钠溶液中滴加稀盐酸时,没有看到明显现象。
(提出问题)氢氧化钠与盐酸是否发生了化学反应?
(查阅资料)酸与碱发生中和反应会放出热量。
(实验设计)甲、乙、丙三位同学分别设计了如下实验方案,请你帮他们完成实验报告
同学 | 实验操作 | 现象 | 结论 |
甲 |
| 溶液由红色变成_____ | 氢氧化钠与盐酸发生了化学反应 |
乙 |
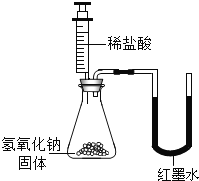
| U形玻璃管中____(填“左”或“右”)边的红墨水液面下降(所加稀盐酸的体积忽略不计) | 氢氧化钠与盐酸发生了化学反应 |
丙 | 用_____测定氢氧化钠溶液的pH;向其中滴加足量的稀盐酸后,再测定溶渡的pH | 最后溶液的pH_____(“≥7”“≤7”或“不变”) | 氢氧化钠与盐酸发生了化学反应 |
(评价反思) 你认为实验设计方案不合理的同学是______,理由是______。
【答案】无 左 pH试纸 ≤ 乙 氢氧化钠固体溶于水也会放出热量
【解析】
[实验设计]甲:氢氧化钠先碱性,使酚酞变为红色,当滴入稀盐酸,稀盐酸与氢氧化钠反应,当恰好完全反应时,溶液显中性,酚酞由红色变为无色;当稀盐酸过量,溶液显酸性,酚酞仍显无色。
乙:氢氧化钠与稀盐酸反应放出热量,锥形瓶中的气体受热膨胀,内压增加,故U形玻璃管中左边液面下降。
丙:溶液的pH用pH试纸测定。加热稀盐酸足量时,溶液中稀盐酸恰好完全反应或稀盐酸过量,故pH≤7。
[评价反思]乙同学的实验不合理,理由是氢氧化钠固体溶于水也会放出热量。

【题目】长郡双语实验中学化学兴趣小组的同学将氢氧化钠溶液和稀硫酸混合,没有观察到明显的现象,他们对此提出了如下问题并进行了相应探究:
问题一:二者之间是否发生了反应?他们设计了如下方案证明二者之间确实发生了反应:
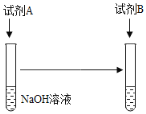
(1)可以选择的试剂组合有____________(填序号)。
①试剂A:足量稀硫酸,试剂B:MgCl2溶液
②试剂A:足量稀硫酸,试剂B:铁粉
③试剂A:少量稀硫酸,试剂B:MgCl2溶液
④试剂A:少量稀硫酸,试剂B:铁粉
(2)小玮认为:若选用_________溶液,不管加入顺序如何,只需控制加入稀硫酸的量也能证明二者发生了反应。
问题二:反应后溶液中溶质有哪些?
(猜想假设)猜想一:只有Na2SO4;猜想二:Na2SO4和NaOH;猜想三:Na2SO4和H2SO4。
(查阅资料)①Na2SO4溶液显中性,②Na2SO4+BaCl2=BaSO4↓+2NaCl。
(实验操作)分别取少量反应后的溶液于试管中,进行如下实验:
实验编号 | 实验过程 | 实验现象 |
① | 加入酚酞溶液 | 不变红 |
② | 加入少量BaCl2溶液 | 产生白色沉淀 |
③ | 加入少量(3)______溶液 | 没有气泡产生 |
(实验结论)猜想一成立。
(实验反思)小光认为,实验(4)________(填实验编号)可省略。小娟取少量反应后的溶液中于试管中,加入红色固体(5)___________(填化学式),观察到红色固体不溶解,也得出了相同结论。
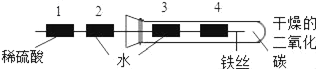
【题目】定性和定量是研究化学实验的两种方法,我们可以通过观察某个实验现象来定性认识,也可以通过称量化学反应前后的质量变化来定量研究。通常瓦斯气体可能含有CO、CO2、CH4等气体,某兴趣小组为确定该气体是否含有这三种气体中的一种或几种,初步设计了如下实验方案供大家讨论:
已知:CH4在加热条件下会与氧化铜反应生成铜、二氧化碳和水。
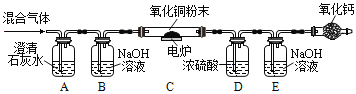
(1)实验过程若发现A处澄清石灰水变浑浊,发生的化学方程式为_____。
(2)同学甲认为,氧化钙的作用是防止空气中的_____对实验造成干扰,小组成员一致同意。
(3)同学乙认为,若装置C中CuO变红,则除了甲烷与CuO可能发生反应外,还可能发生的反应是_____;(用化学方程式表示)。
(4)装置B中装有足量NaOH溶液,其作用是: _____。
(5)同学丙认为,欲通过D装置中浓硫酸因吸收水分而增重,说明混合气体中含有CH4的思路不严密,认为需要在_____ (填序号) 间再增加一个装有_____的洗气瓶 (编号为F),才能证明含有CH4。
(6)同学丁认为该装置存在着重大安全隐患,理由是_____。综合上述讨论,兴趣小组将经过处理后的混合气体,通过改进后的装置进行了实验探究,请根据实验现象和数据填写结论:
装置 | 实验现象/数据 | 实验结论 |
A | 石灰水变浑浊 | 通过实验现象和数据,小组成员一致认为该气体样品中含有_____。 |
B | 无明显现象 | |
C | 黑色粉末变成红色 | |
D | 装置D增重1.8g | |
E | 装置E增重2.2g |
【题目】将一定量的丙烷(C3H8)和氧气置于一个密闭的容器中引燃并充分反应,测得反应前后各物质的质量如表所示,下列判断不正确的是( )
物质 | C3H8 | O2 | H2O | CO2 | X |
反应前质量/g | 4.4 | 12.8 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 7.2 | 4.4 | a |
A.表中a的值一定是5.6
B.若8.8g丙烷完全反应,则生成14.4g水
C.生成物X中一定含有氢元素
D.若4.4g丙烷与16.0g氧气充分反应,则无X生成