题目内容
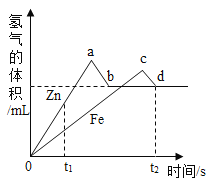
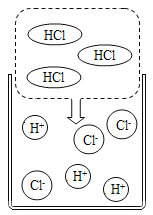
【题目】(1)如图是某同学査阅的氯化氢气体溶于水的示意图。从微观角度分析氯化氢气体不显酸性的原因是_____________。
(2)用硫酸铜配制农药波尔多液,溶解硫酸铜时不宜用铁制容器。用化学方程式表示其原因:___________。
【答案】在氯化氢气体中,氯化氢气体是由氯化氢分子构成的,没有解离出的氢离子,所以氯化氢气体不显酸性 Fe+CuSO4=Cu+FeSO4
【解析】
(1)在氯化氢气体中,氯化氢气体是由氯化氢分子构成的,没有解离出的氢离子,所以氯化氢气体不显酸性;
(2)波尔多液主要由硫酸铜和氢氧化钙混合配制而成,不能用铁制品盛放的原因是由于铁会与硫酸铜反应生成铜和硫酸亚铁,反应的化学方程式为:Fe+CuSO4=Cu+FeSO4。

练习册系列答案
相关题目
【题目】如图装置可以以完成多个简单实验,具有药品用量少、实验现象明显、尾气 不外逸等优点。

(1)若甲中吸有浓氨水,乙中吸有无色酚酞溶液,将甲、乙中的液体同时挤出,一段时 间后,可观察到挤入到烧杯②中的无色酚酞溶液______,说明分子具有的性质是______
(2)若先将甲中的液体挤出,观察出气球明显鼓起,一段时间后恢复原状,再将乙中的液体挤出,气球又明显鼓起,过一会略缩小,但不会恢复到原状,请将下表中的试剂补充完整。
滴管甲 | 烧杯① | 滴管乙 | 烧杯② | |
试剂 | H2O | ______ | ______ | Mg |
图示气球鼓起是因为装置内气压增大,第二次气压增大的原因是______。
(3)若甲中吸有水,乙中吸有稀硫酸,烧杯①中盛有用石蕊溶液染成紫色的干燥纸花,烧杯②中盛有碳酸钠 粉末,为了验证使石蕊变色的物质是碳酸而不是二氧化碳,应进行实验操作的是______。