题目内容
【题目】2019 年政府工作报告中提出今年工作重点之一是加强污染防治和生态建设,大力推动绿色发展,要求 SO2、NOx 排放量下降 3%。工业上常用 NaOH 溶液来吸收二氧化硫以达到防治污染的目的。
(1)酸雨的 pH_________5.6(填“<”、“=”或“>”),危害性大。地球不想吃“酸”, 请你写出一条防治酸雨的做法:____________。
(2)如图是喷淋塔吸收二氧化硫的图示
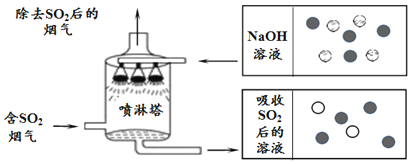
①吸收过程用氢氧化钠溶液喷淋 SO2,而不是 SO2 直接通入氢氧化钠溶液是为了_______________。
②写出 NaOH 溶液吸收 SO2 的化学方程式__________________。
③上图中小球分别表示 NaOH 溶液及吸收 SO2 后所得溶液中溶质的微粒,其中“ ![]() ”表示的微粒是_____________(填符号)。
”表示的微粒是_____________(填符号)。
【答案】< 提倡人们使用脱硫煤 增大气液接触面积,提高 SO2 吸收效果 2NaOH+SO2 = Na2SO3 + H2O Na+
【解析】
(1)酸雨是pH小于5.6的雨水;酸雨中的酸绝大部分是硫酸和硝酸,主要来源于工业生产和民用生活中燃烧煤炭或石油等排放的,以及汽车尾气释放的硫氧化物(主要是二氧化硫)、氮氧化物(主要是二氧化氮)等酸性物质。防治酸雨方法可以是提倡人们使用脱硫煤等。
(2)①吸收过程用氢氧化钠溶液喷淋 SO2,而不是 SO2 直接通入氢氧化钠溶液是为了增大气液接触面积,提高 SO2 吸收效果;
②NaOH与SO2 反应生成亚硫酸钠和水,反应的化学方程式为:2NaOH+SO2 = Na2SO3 + H2O;
③NaOH与SO2 反应时,溶液中的钠离子没有改变。上图中小球分别表示 NaOH 溶液及吸收 SO2 后所得溶液中溶质的微粒,其中“ ![]() ”表示的微粒是Na+。
”表示的微粒是Na+。

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案【题目】下图是用氯化钠溶液和氯化钾溶液制取氯酸钾的工艺流程,请根据题意回答下列问题。
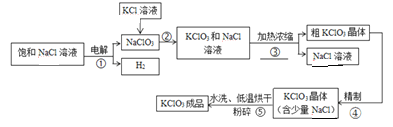
【资料】氯酸钾和氯化钠部分温度下的溶解度如下:
10℃ | 20℃ | 30℃ | 40℃ | |
氯酸钾 | 5.0g | 7.4g | 10.0g | 14.0g |
氯化钠 | 35.8g | 36.0g | 36.3g | 36.6g |
(1)请写出步骤②的化学方程式_________,该反应的基本反应类型是_________________。
(2)步骤③的操作分别是_________、过滤(填操作名称)。
(3)步骤⑤中是采用20℃以下的水进行洗涤,目的是①除去少量氯化钠②_____________。
(4)步骤⑤采用低温烘干,为什么不采用高温烘干___________________________(用化学方程式表示)。