题目内容
【题目】实验室常用氯酸钾和二氧化锰制取氧气(装置A),也可用过氧化氢溶液和二氧化锰粉末来制取氧气(装置B)。请回答下列问题:
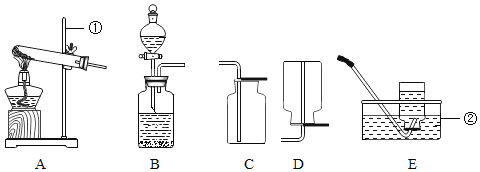
(1)写出带标号仪器的名称:①_____;②_____
(2)向气体发生装置内加入药品前,应该进行的操作是_____
(3)用向上排空气法收集氧气,并用带火星的木条放在集气瓶口,检验氧气是否收集满,这是利用了氧气的_____性质。
(4)用排水法收集氧气时,看到_____,说明氧气已集满;若用排水法收集的氧气中含有氮气的原因可能是_____(写一点即可)
(5)二氧化碳是一种能溶于水,密度大于空气的密度,收集二氧化碳应选择的装置是_____。
(6)若选用B装置制取氧气时,写出该反应的化学方程式_____。
(7)实验室用块状硫化亚铁和稀硫酸反应就有硫化氢气体产生,硫化氢气体比空气重,能溶于水。则实验室制备硫化氢气体的发生装置应选用_____,收集装置可选用_____。
(8)由此我们得到启示:实验室选择气体发生装置时,应考虑_____和_____;选择气体收集装置时,应考虑_____和_____。
【答案】铁架台 水槽 检查装置的气密性 密度比空气大、助燃 集气瓶口有气泡冒出 导管口刚冒出气泡就开始收集气体 C 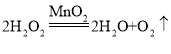 B C 反应物状态 反应条件 气体的密度 在水中的溶解性
B C 反应物状态 反应条件 气体的密度 在水中的溶解性
【解析】
过氧化氢在二氧化锰催化作用下生成水和氧气,稀盐酸和碳酸钙反应生成氯化钙、水和二氧化碳,硫化亚铁和稀硫酸反应生成硫酸亚铁和硫化氢。
(1)仪器①是铁架台,②是水槽。
(2)向气体发生装置内加入药品前,应该进行的操作是检查装置的气密性。
(3)用向上排空气法收集氧气,说明氧气的密度比空气大,用带火星的木条放在集气瓶口,检验氧气是否收集满,说明氧气具有助燃性。
(4)用排水法收集氧气时,看到集气瓶口有气泡冒出时,说明氧气已集满;若用排水法收集的氧气中含有氮气的原因可能是集气瓶没有事先装满水,或导管口刚冒出气泡就开始收集气体。
(5)二氧化碳是一种能溶于水,密度大于空气的密度,收集二氧化碳应选择向上排空气法;故收集装置选用C。
(6)装置B适用于固液常温下制取气体,即过氧化氢在二氧化锰的催化作用下制取氧气,同时生成水,化学方程式为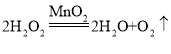 。
。
(7)实验室用块状硫化亚铁和稀硫酸制取硫化氢气体,属于固液常温型,选择装置B来制取,硫化氢气体密度比空气大,能溶于水,所以可用向上排空气法来收集;故收集装置选用C。
(8)实验室选择气体发生装置时,应考虑反应物的状态和反应条件;选择气体收集装置,一般考虑气体物理性质中的密度和溶解性。

【题目】实验室部分装置如图所示,请回答下列问题:
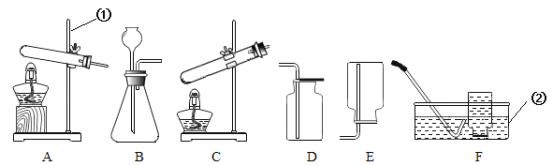
(1)写出标号仪器的名称:①_______________;②_____________。
(2)制取氧气有很多种方法,如分解过氧化氢溶液、加热高锰酸钾、_______等。
(3)采用分解过氧化氢溶液制取氧气有许多优点,如:______(填序号)。
①产物无污染 ②不需加热 ③需加热 ④生成物只有氧气
(4)选择发生和收集O2的装置,填写在下表中(填字母)。
选用药品 | 发生装置 | 收集装置 |
过氧化氢溶液、二氧化锰 | ________ | ___________ |
高锰酸钾 | _________ |
(5)如果用二氧化锰与浓硫酸加热制备O2,可选用的发生装置是______(填字母)。
(6)选用E装置收集气体时,下列实验操作正确的是________(填序号)。
①反应前,将集气瓶注满水,用玻璃片盖着瓶口,倒立在盛水的水槽中
②开始反应后,等到气泡连续且均匀时,再将导管口移入集气瓶
③收集气体后,将集气瓶盖上玻璃片再移出水槽
(7)实验室用高锰酸钾制备O2的文字表达式是________。
【题目】下图1为实验室用一氧化碳还原氧化铜的实验装置图,某兴趣小组在老师的指导下按下图连接装置、检查装置的气密性、装药品、固定装置。但就下面的实验操作顺序问题出现了分歧:小丽认为先通一段时间CO排净空气,然后再点燃A处酒精灯和C处酒精灯,小亮觉得这样做不好,他的理由是:_____;小亮主张先点燃A处酒精灯和C处酒精灯,然后再通CO,小菊又提出反对,她的理由是:_____,老师认他们的反对意见都有道理。请你帮助这两位同学解决他们的困难,你的办法是:_____。
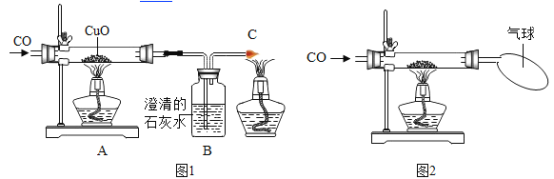
小红为了探究CO是否能还原CuO,做了如图2所示的实验。实验发现CO与CuO加热后黑色粉末变成红色粉末。请你参与该研究过程:
[研究课题]探究红色粉末的主要成分
[查阅资料]
(1)有关物质的颜色:Cu:红色,CuO:黑色,Cu2O:红色,CuSO4溶液:蓝色。
(2)CuO和Cu2O都能和稀硫酸发生反应,化学方程式为:
CuO十H2SO4=CuSO4+H2O; Cu2O+H2SO4=CuSO4+Cu+H2O
[猜想与实验]
(1)如果硬质玻璃管内红色粉末为一种物质,请猜想它的成分,并设计简单的实验证明你的猜测。
猜想 | 简单实验方案 | 现象 | CO和CuO反应的化学方程式 |
_____ | _____ | _____ | _____ |
_____ | _____ | _____ | _____ |