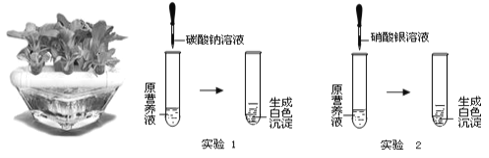
题目内容
【题目】某研究性学习小组在验证“碱使酚酞试液变红”的实验时,发现一个意外现象:将酚酞试液滴人某NaOH溶液中,溶液变成了红色,可是过一会儿红色却消失了。
【提出问题】是什么原因导致滴有酚酞的NaOH溶液由红色褪为无色?
【猜想与假设】他们分别对这种意外现象作如下猜想:
甲同学:可能是酚酞与O2发生了反应;
乙同学:可能是NaOH溶液与空气中的CO2发生了反应;
丙同学:可能与NaOH溶液浓度大小有关;
你认为可能还与_________________________________有关(写一条即可)。
【设计实验】三位同学分别设计实验验证自己的猜想:
(1)甲同学设计了如下实验,请你填写下表。
实验步骤 | 设计这一步骤的目的 | 实验现象 | 实验结论 |
1.将NaOH溶液加热煮沸 | 溶液变红,过一会儿红色消失 | 甲同学猜想___________(填“正确”或不正确”) | |
2.向冷却后的溶液中滴人酚酞,并滴一些植物油在其上方 |
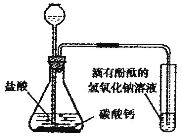
(2)乙同学设计如图装置进行实验,一段时间后,试管中溶液的红色褪去,于是认定自己的猜想正确。请写出CO2与NaOH溶液反应的化学方程式:________________________。甲同学认为乙同学的实验不够严谨,理由是________________________。
(3)丙同学使用了色度传感器测溶液的颜色。他在a、b、c三个比色皿中分别加入等量5%、10%、20%的NaOH1溶液,然后各滴加2滴酚酞试液。溶液颜色的变化曲线如图[说明:溶液无色时色度值(透过率)为100%]。请你观察下图回答问题。①写出两条规律性结论:___________________________________________________;
___________________________________________________。
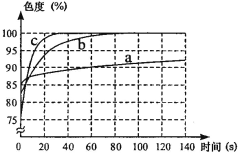
②推测5%的NaOH溶液滴加2滴酚酞试液后褪为无色的时间约为
A.小于30s
B.30-90s
C.90-140s
D.140-180s
E.180-280s
F.大于280s
【答案】【猜想与假设】仪器不干净,含有酸性物质
【设计实验】(1)
实验步骤 | 设计这一步骤的目的 | 实验现象 | 实验结论 |
除去溶液中的氧气 | 甲同学猜想不正确_ | ||
隔绝氧气 |
(2)2NaOH+CO2 =Na2CO3+H2O
若制取的二氧化碳气体中混有氯化氢气体,试管中溶液的红色也能褪去
(3)①氢氧化钠溶液的浓度越大,酚酞试液变红后褪色越快;氢氧化钠溶液的浓度越小,色度值越大
②F
【解析】
试题分析:【猜想与假设】导致滴有酚酞的NaOH溶液由红色褪为无色的可能原因:仪器不干净,含有酸性物质,将NaOH溶液中和了
【设计实验】(1)为了验证甲同学:可能是酚酞与O2发生了反应的这个假设,可以让滴有酚酞的NaOH溶液给隔绝氧气,看是否红色会褪去
实验步骤 | 设计这一步骤的目的 | 实验现象 | 实验结论 |
除去溶液中的氧气 | 甲同学猜想不正确_ | ||
隔绝氧气 |
(2)CO2与NaOH溶液反应的化学方程式:2NaOH+CO2 =Na2CO3+H2O;甲同学认为乙同学的实验不够严谨,理由是:若制取的二氧化碳气体中混有氯化氢气体,试管中溶液的红色也能褪去
(3)通过观察溶液颜色的变化曲线图,可总结两条规律性结论:①氢氧化钠溶液的浓度越大,酚酞试液变红后褪色越快;氢氧化钠溶液的浓度越小,色度值越大
② 根据通过观察溶液颜色的变化曲线图,5%的NaOH溶液滴加2滴酚酞试液,刚开始的色度值为85%,当时间过了140s后,色度值还不到92.5%,故要使色度值达到100%,故所需的时间至少需要2×140s ,故选F