题目内容
【题目】有A、B、C、D四种元素,A的原子核外有3个电子层,且第3电子层上的电子数比第2电子层的电子数少1;B元素的某氧化物分子组成为BO3,其中B元素与氧元素的质量比为2:3,且B原子核内质子数与中子数相等(已知:元素的相对原子质量近似等于质子数加上中子数);C﹣和D2+的电子层结构与氖原子相同.
(1)写出下列微粒的符号:C﹣_____、D2+_____
已知①通常电子层数越多,微粒半径越大;②核电荷数越大,对核外电子吸引力越强,微粒半径越小.试比较以上两种离子半径的大小_____
(2)B元素形成常见单核离子的化学符号:_____,写出BO3与水反应的方程式_____
(3)已知:活泼的非金属单质能把相对不活泼的非金属单质从它的化合物中置换出来.已知A的单质比I2活泼,写出A的单质与KI反应的方程式_____.
【答案】F﹣ Mg2+ F﹣>Mg2+ S2﹣ ![]()
![]()
【解析】
A元素的原子有三个电子层,第三层电子数比第二层少1,由于第二层容纳8个电子,故A元素的原子最外层有7个电子,核电荷数=2+8+7=17,所以A为氯元素;
根据B元素与氧元素的质量比=B的相对原子质量:O的相对原子质量×3=2:3,B元素的相对原子质量=48×2÷3=32,B原子核内质子数与中子数相等,则B元素的质子数为32÷2=16,所以B为硫元素;
C﹣和D2+的电子层结构与氖原子相同,氖的原子序数为10,C得到一个电子核外电子数为10,C的质子数为9,则C为氟元素,D失去两个电子核外电子数为10,D的质子数为12,则D为镁元素;
(1)C为氟元素,D为镁元素,故C﹣:F-;D2+:Mg2+;
F-和Mg2+的电子层数都是2,F-的核电荷数为9,Mg2+的核电荷数为12,核电荷数越大,微粒半径越小,故两种离子的半径大小为:F﹣>Mg2+;
(2)硫元素最外层电子数为6,易得到两个电子,从而带上两个单位负电荷,故B元素形成常见单核离子的化学符号为S2﹣;
BO3为SO3,SO3与水反应生成硫酸,该反应的化学方程式为:![]() ;
;
(3)A为氯元素,A的单质为氯气,已知活泼的非金属单质能把相对不活泼的非金属单质从它的化合物中置换出来,故氯气和碘化钾反应生成氯化钾和碘,化学方程式为:![]() 。
。

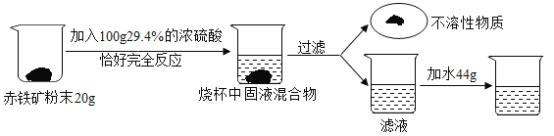
【题目】废铁屑主要成分是铁,还有少量铁锈(Fe2O3),硫酸亚铁的生产工艺如图所示。
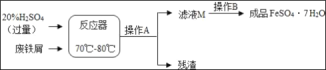
(1)在反应器中除发生Fe2O3+3H2SO4=Fe2(SO4)3+3H2O,Fe2(SO4)3+Fe═3FeSO4这两个反应外,还会发生另外一个反应,化学方程式为:_____,反应器要加强通风,严禁烟火,其原因是:_____。
(2)将成品在有氧条件下焙烧,可转化为Fe2O3、SO2和SO3.为了提高SO3的产率,某实验小组进行了系列探究,实验数据如下:
编号 | 空气通入量/Ls﹣1 | 温度/℃ | SO2产率% | SO3产率/% |
a | 0.02 | 850 | 45.4 | 54.6 |
b | 0.06 | 850 | 30.5 | 69.5 |
c | 0.10 | 810 | 11.1 | 88.9 |
d | 0.10 | 850 | 11.1 | 88.9 |
e | 0.10 | 890 | 11.2 | 88.8 |
①本实验主要研究了哪些因素对SO3产率的影响_____。
②根据上表数据,生产过程中采用实验_____(填编号)的提取条件最合理。
③分析上表数据,空气的通入量对SO3的产率的影响规律是_____。
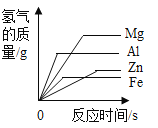
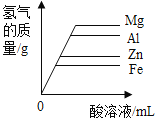
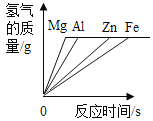
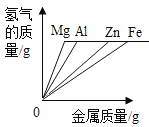
【题目】镁、铝、锌、铁与稀盐酸或稀硫酸之间的反应规律及图象正确的是( )
|
|
|
|
A等质量的镁、铝、锌、铁与足量酸反应,氢气质量与反应时间的关系图象 | B等质量的镁、铝、锌、铁与足量酸反应,氢气质量与酸溶液的关系图象 | C等量酸与足量镁、铝、锌、铁反应,氢气质量与反应时间的关系图象 | D等量酸与足量镁、铝、锌、铁反应,氢气质量与金属质量的关系图象 |
A.AB.BC.CD.D