题目内容
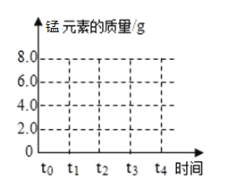
【题目】实验室用氯酸钾和二氧化锰的固体混合物粉末共33.2g加热制取氧气,记录产生氧气的质量与加热时间如图所示,请回答下列问题:
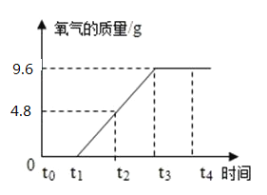
(1)t0-t1时段氧气质量为0,其原因是________________;t3-t4时段内剩余固体物质的质量为_______g。
(2)请根据图中数据计算原混合物中氯酸钾的质量________。
(3)请在图坐标中,画出固体中锰元素质量在t0-t4时段变化示意图________。
【答案】没有达到分解温度 23.6 24.5g 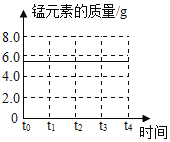
【解析】
根据质量守恒定律可知,过程中质量的减少是因为生成了氧气,所以可以求算氧气的质量,根据氧气的质量和对应的化学方程式求算原固体混合物中氯酸钾的质量。
解:(1)t0→t1时段氧气质量为0,其原因是 没有达到分解温度;t3→t4时段内剩余固体物质的质量为33.2g-9.6g=23.6g;
(2)设原混合物中氯酸钾的质量为x,
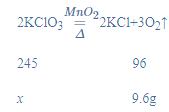
![]()
x=24.5g;
(3)则二氧化锰的质量为33.2g-24.5g=8.7g,其中锰元素的质量为8.7g×![]() ×100%=5.5g。在t0→t4时锰元素质量一直不变,为5.5g,画出固体中锰元素质量在t0→t4时为:
×100%=5.5g。在t0→t4时锰元素质量一直不变,为5.5g,画出固体中锰元素质量在t0→t4时为: 。
。

 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案【题目】某化学兴趣小组的同学,为了比较金属R与铁、铜的金属活动性强弱,进行如下探究活动:
[查阅资料]铁的活动性比铜强.
[进行猜想]对三种金属的活动性顺序做出如下猜想:
猜想一:R>Fe>Cu; 猜想二:_______________; 猜想三:Fe>Cu>R
[收集证据]为了验证哪一种猜想成立,甲、乙、丙三位同学分别展开实验探究.
主要操作 | 主要现象 | 实验结论 | |
甲 | 将打磨好的R丝插入盛有硫酸铜溶液的试管中 | ______________ | 猜想一 正确 |
乙 | 将粗细相同打磨好的R丝、铁丝,分别插入体积和溶质质量分数都相同的稀盐酸中 | R丝表面产生气泡速率比铁丝表面产生气泡速率___(填“快”或“慢”) | |
丙 | 将粗细相同打磨好的R丝、铁丝,分别在空气中点燃 | R丝在空气中剧烈燃烧,铁丝在 空气中______ |
写出铁丝在氧气中燃烧的化学方程式__________________________________
[交流反思]三位同学交流讨论后认为,比较金属活动性强弱的方法有多种.
[归纳总结]他们总结得出比较金属活动性强弱的常见方法有:
(1)金属与氧气反应的难易和剧烈程度;
(2)金属与酸溶液是否反应或反应的剧烈程度;
(3)金属与_____是否反应.