题目内容
【题目】某工业废水中含有大量的硫酸亚铁、少量的硫酸铜和污泥。某同学设计了一个既经济又合理的方法回收铜和硫酸亚铁晶体,方案流程如图。
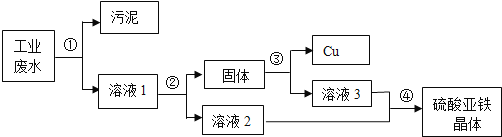
(1)步骤①操作名称为______,步骤②中,需要加入过量的______,以确保完全置换出硫酸铜中的铜元素。
(2)为了得到纯净的铜和硫酸亚铁,步骤③中需要加入适量的物质是______。
(3)本工业流程涉及到的两个化学反应基本反应类型为______。
(4)写出步骤②所涉及的化学方程式______。
【答案】过滤 铁 稀硫酸 置换反应 ![]()
【解析】
(1)过滤分离不溶性固体与液体,将废水中的污泥与溶液用过滤法分离,步骤①的操作为过滤;要将硫酸铜与硫酸亚铁的混合溶液中回收铜,同时得到硫酸亚铁溶液,只能加入过量的铁置换硫酸铜溶液中的铜;
(2)铁与硫酸铜反应生成铜和硫酸亚铁,因此经过步骤②之后得到的固体中含有生成的铜和剩余的铁,加入适量稀硫酸与铁反应生成硫酸亚铁;
(3)本工业流程涉及到的两个化学反应为铁和硫酸铜,铁和硫酸反应,两个反应的基本类型为置换反应;
(4)步骤②发生反应为铁和硫酸铜反应生成硫酸亚铁和铜单质,反应的化学方程式为Fe+CuSO4=FeSO4+Cu;

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目