题目内容
【题目】质量守恒定律是化学反应中的重要规律,我能运用此规律解答下列问题:
(1)某纯净物X在空气中完全燃烧,反应的化学方程式为:X+3O2=2CO2+3H2O(反应条件已略去),则X的化学式为 .
(2)在催化剂并加热的条件下,A与B反应生成C和D.反应前后分子变化的微观示意图所下所示:
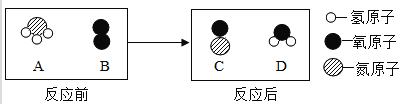
①下列说法正确的是 (填序号).
a.该反应类型为置换反应
b.4种物质中只有D属于氧化物
c.反应前后,氮元素化合价升高
d.化学反应中分子可以再分,而原子不能
②该反应的化学方程式为 .
【答案】(1)C2H4 (2)①abcd ②4NH3+3O2![]() 2N2+6H2O
2N2+6H2O
【解析】
试题分析::(1)根据反应前后原子的种类和数目都不变:X+3O2═2CO2+2H2O,可以知道反应后有2个C,4个H,6个O,而反应前只出现了6个O,故X中含有2个C,4个H,化学式为C2H4.(2)根据质量守恒定律反应前后原子的种类和数量不变,配平方程式,故化学方程式为:4NH3+3O2![]() 2N2+6H2O
2N2+6H2O
a、根据置换反应是指一种单质与一种化合物反应,生成另一种单质和另一种化合物的反应,故a正确;
b、根据氧化物是指由两种元素组成,其中一种为氧元素的化合物,可知b正确;
c、反应前,氮元素显﹣3价,反应后,氮元素显0价,故c正确;
d、化学反应中分子可以再分,而原子不能再分正确;故选abcd

练习册系列答案
相关题目