题目内容
【题目】为了测定某化工厂由氯化钡和氯化钠组成的产品中氯化钠 的成分。小明取16.25g固体样品,全部溶于143.6g水中,向所得到的混合溶液中逐滴加入溶质质量分数为10.6%的碳酸钠溶液,记录如下图所示的曲线关系。
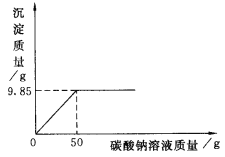
求:(1)产品中氯化钠的质量分数;
(2)当氯化钡与碳酸钠恰好完全反应时,所得溶液中
溶质的质量分数。
【答案】(1)36% (2)5.85%
【解析】
试题分析:在氯化钡和氯化钠的混合溶液中逐滴加入碳酸钠溶液,发生反应:BaCl2+Na2CO3==BaCO3↓+2NaCl;故结合图像可知:当加入的碳酸钠溶液质量为50g时,反应刚好结束,所得BaCO3沉淀质量为9.85g,
解:设样品中BaCl2的质量为x,生成NaCl的质量为y.
Na2CO3 + BaCl2 = BaCO3↓+2NaCl
106 208 117
50g×10.6% x y
(1)106:208= 50g×10.6%:x
x=10.4g
产品中NaCl的质量分数=(16.25g-10.4g)/16.25g×100%=36%
(2)106:117=50g×10.6%:y
y=5.85g
溶液中溶质NaCl的总质量=16.25g-10.4g+5.85g=11.7g
溶液的总质量=16.25g+143.6g+50g-9.85g=200g
所得溶液中溶质的质量分数=11.7g/200g×100%=5.85%
答:略

 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案【题目】下列关于水的叙述,错误的是
A、电解水时,与电源正极相连的玻璃管内得到的气体能在空气中燃烧
B、水是由氢元素和氧元素组成的
C、生活中通过煮沸可降低水的硬度
D、净化水的方法有吸附、沉淀、过滤和蒸馏等
【题目】(7分)一次趣味化学活动中,王老师向同学们展示了一瓶标签受损的无色溶液,如下图所示。
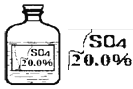
要求同学们进行探究:
确认这瓶溶液到底是什么溶液?
提出猜想:王老师提示:这瓶无色溶液只能是以下四种溶液中的一种:
①硫酸镁溶液、 ②硫酸钠溶液、
③硫酸溶液、 ④硫酸铵溶液。
查阅资料:
A:常温下,相关物质的溶解度如下
物质 | MgSO4 | Na2SO4 | (NH4)2SO4 | H2SO4 |
溶解度 | 35.1g | 19.5g | 75.4g | 与水任意比互溶 |
B:(NH4)2SO4的水溶液显酸性
【实验探究】
(1)通过查阅资料,小明同学认为猜想 (填序号)不成立,原因是 。
(2)为确定其它几种猜想是否正确,小明同学继续进行探究:
实验步骤 | 实验现象 | 实验结论 |
a取该溶液少许于试管中,向其中滴加几滴氢氧化钠溶液 | 溶液中有白色沉淀生成 | 猜想①成立 |
b取该溶液少许于试管中,向其中滴加几滴紫色石蕊溶液 | 猜想③成立 |
小芳同学认为小明实验步骤b的结论不正确,她的理由是 ;
(3)请你设计实验方案,确认该溶液是硫酸铵溶液并完成实验报告:
实验操作 | 实验现象 | 实验结论 |
取该溶液少许于试管中,再往该溶液加入 溶液,加热。 | 猜想④成立,该反应的化学方程式为 |