题目内容
【题目】小明在市场看到,鱼老板将一勺白色粉末加入水中,水中奄奄一息的鱼很快张开嘴,活蹦乱跳起来,小明对这种“白色粉末”很感兴趣,与小刚进行了相关探究。
(查阅资料)这种“白色粉末”的主要成分是过碳酸钠(化学式为Na2CO4),常温下,与水反应生成氧气。
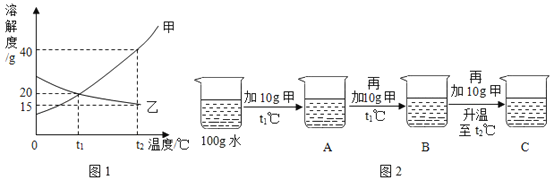
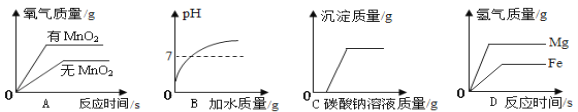
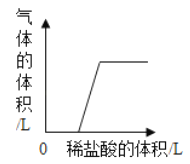
(实验1)小明选用如图所示装置中的_____(选填序号)进行过碳酸钠与水的反应并收集产生的气体,经检验该气体是氧气,检验方法是_____。
A  B
B 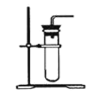
C 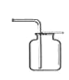 D
D 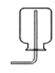
(提出问题)过碳酸钠与水反应后得到的溶液M中溶质的成分是什么?
(作出猜想)根据过碳酸钠与水的组成作出三种猜想。
猜想一:碳酸钠;猜想二:氢氧化钠;猜想三:碳酸钠和氢氧化钠。
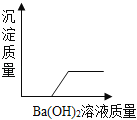
(实验2)小明取溶液M,滴加氯化钙溶液,观察到有白色沉淀生成,他认为白色沉淀是碳酸钙,溶液中一定含有碳酸钠。小刚提出质疑,产生的白色沉淀不一定是碳酸钙,他的理由是:_____。
(实验3)小刚取溶液M,滴加稀盐酸,观察到_____,证明溶液中一定含有碳酸钠,从而否定了猜想二。碳酸钠与稀盐酸反应的化学方程式为_____。
(实验4)为进一步确定溶液M中是否含有氢氧化钠,他们向溶质M中滴加氯化钙溶液至不再产生沉淀为止,取上层溶液,加入_____,无明显现象,证明溶液中无氢氧化钠溶液,猜想一正确。该实验中用氯化钙溶液而不用饱和石灰水,原因是_____。
(反思拓展)
(1)根据过碳酸钠的性质,应_____保存。
(2)检验A、B两种物质是否同时存在,一定要考虑二者性质的互相干扰问题。
【答案】BC 将带火星的木条伸入集气瓶中,带火星的木条复燃,说明气体是氧气 氯化钙与氢氧化钠反应,生成微溶性的氢氧化钙 有气泡产生 Na2CO3+2HCl=2NaCl+H2O+CO2↑ 无色酚酞溶液 碳酸钠能与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,无法证明原溶液中否含有氢氧化钠 密封
【解析】
过碳酸钠与水反应,属于固液常温型,氯化钙与氢氧化钠反应,生成微溶于水的氢氧化钙,碳酸钠与盐酸反应,产生二氧化碳气体,酚酞试液在碱性溶液中为红色、碳酸钠能与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠。
过碳酸钠与水反应,属于固液常温型,氧气密度比空气大,应选装置中的BC进行过碳酸钠与水的反应并收集产生的气体;经检验该气体是氧气,检验方法是将带火星的木条伸入集气瓶中,带火星的木条复燃,说明气体是氧气。
产生的白色沉淀不一定是CaCO3,可能是氯化钙与氢氧化钠反应,生成微溶性的氢氧化钙。
小刚取溶液M,滴加稀HCl,观察到产生气泡,证明溶液中一定含有Na2CO3,Na2CO3与稀HCl反应生成氯化钠、水和二氧化碳,反应的化学方程式为:
Na2CO3+2HCl=2NaCl+H2O+CO2↑。
为进一步确定溶液M中是否含有NaOH,向溶液M中滴加CaCl2溶液至不再产生沉淀为止,取上层溶液,加入酚酞溶液,无明显现象,证明溶液中无NaOH,猜想一正确,该实验中用CaCl2溶液而不用饱和石灰水,原因是碳酸钠能与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,无法证明原溶液中是否含有氢氧化钠。
[反思拓展]
(1)过碳酸钠能和水反应,而空气中含有水蒸气,因此应该密封保存。

 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案【题目】铜镁合金常用作飞机天线等导电材料。欲测定合金的组成(其他元素忽略不计),进行了以下实验:取出3g合金样品,将60g稀硫酸分为6等份依次加入样品中,充分反应后过滤、洗涤、干燥、称重,得到的实验数据如下:
稀硫酸用量 | 第1份 | 第2份 | 第3份 | 第4份 | 第5份 | 第6份 |
剩余固体质量 | 2.5g | m | 1.5g | 1.0g | 0.6g | 0.6g |
(1)铜镁合金属于_____(填“混合物”或“纯净物“);
(2)加入稀硫酸发生反应的化学方程式为_____;
(3)分析数据可知表格中m=_____;
(4)合金样品中铜的质量分数是_____;
(5)若反应过程中产生的气体收集起来,可得到氢气的质量为多少g?_____