题目内容
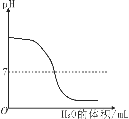
【题目】如图为A、B、C三种物质的溶解度曲线。请根据图回答:
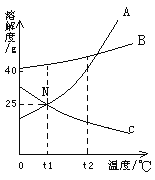
(1)N点的意义:______
(2)t1℃时,在25g水中放入20g A 物质,形成的A溶液溶质质量分数是_________,要使该溶液变为不饱和溶液可采用的方法 ________(填一种即可)
(3)t2℃时,将等质量的A、B、C三种物质的饱和溶液,降温至t1℃,析出晶体最多的是______,没有晶体析出的是______。
(4)t2℃时,将等质量的A、B、C三种物质的饱和溶液,均恒温蒸发等质量的水,析出晶体由多到少的顺序为________________;
(5)欲将混有少量B的A物质提纯,可以采取的措施是____________________。
(6)t2℃时,将A、B、C的饱和溶液降温至t1℃,A、B、C的溶液溶质质量分数大小关系是_______________。
(7)上图中可能是气态物质的溶解度曲线是________。
【答案】在t1℃时,A和C的溶解度相等,且为25g 20% 添加溶剂 A C B>A>C 加热浓缩,冷却结晶 B>A>C C
【解析】
(1)由溶解性曲线图可知,N点的意义可以表示为在t1℃时,A和C的溶解度相等,且为25g。故填:在t1℃时,A和C的溶解度相等,且为25g。
(2)t1℃时,A 物质的溶解度为25g,即在100g水中能溶解25g,而在25g水中放入20g A 物质只能溶解25:100=x:25=6.25g,形成的A溶液溶质质量分数是![]() ,要使该溶液变为不饱和溶液可采用的方法有升高温度,添加溶剂。故填:20%;添加溶剂
,要使该溶液变为不饱和溶液可采用的方法有升高温度,添加溶剂。故填:20%;添加溶剂
(3)由于A的溶解度随温度的降低而减小,且受温度的影响最大,C物质随温度的降低而升高,可知t2℃时,将等质量的A、B、C三种物质的饱和溶液,降温至t1℃,析出晶体最多的是A物质,没有晶体析出的是C物质。故填:A;C
(4)t2℃时,溶解度由大到小的顺序为B>A>C,本题实际考差的是溶解度的比较,若将等质量的A、B、C三种物质的饱和溶液,均恒温蒸发等质量的水,析出晶体由多到少的顺序为B>A>C;故填:B>A>C
(5)由于A的溶解度随温度的降低而减小,且受温度的影响最很大,B受温度的变化溶解度变化不大,欲将混有少量B的A物质提纯,可以采取的措施是加热浓缩,冷却结晶,过滤,即可得到纯的A物质。故填:加热浓缩,冷却结晶
(6)由于A的溶解度随温度的降低而减小,且受温度的影响最很大,故从t2℃降至t1℃时,A物质析出晶体最多,溶解度降至小于B,此时为饱和溶液;B随温度的降低溶解度变化不大,故析出的晶体较少,此时比A的溶解度大,此时为饱和溶液;而C物质随着温度降低溶解度升高,由于没有C物质继续溶解,C物质的质量分数与变化前相等,此时为不饱和溶液;故t2℃时,将A、B、C的饱和溶液降温至t1℃,A、B、C的溶液溶质质量分数大小关系是B>A>C。故填:B>A>C
(7)气态物质的溶解度随着温度升高,溶解度下降,由图可知C曲线符合。故填:C

 阅读快车系列答案
阅读快车系列答案