题目内容
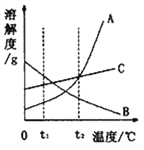
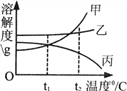
【题目】下图是甲、乙、丙三种物质(均不含结晶水)的溶解度曲线。现有t2℃时甲、乙、丙三种物质的饱和溶液(无固体存在),请根据右图回答:
(1) t2℃时,将三种饱和溶液分别恒温蒸发相同质量的水,析出晶体最多的是______;
(2)将三种饱和溶液分别从t2℃降温到t1℃时,所得溶液中溶质的质量分数由大到小的顺序为______。
【答案】 甲 乙>甲=丙。
【解析】(2)t2℃时三种物质的溶解度由大到小的顺序依次是甲、乙、丙,即等量的水中溶解的甲最多,所以将三种饱和溶液分别恒温蒸发相同质量的水,析出晶体最多的是甲;
(3)根据溶解度的定义和溶质的质量分数的关系可以知道,在t2℃时,甲的溶解度最大,所以其饱和溶液的溶质的质量分数也最大,丙的溶解度最小,其饱和溶液的溶质的质量分数也最小,即在t2℃时三种饱和溶液的溶质的质量分数由大到小顺序为:甲>乙>丙;但是将温度从t2℃降温到t1℃时,甲的溶解度比乙的溶解度变化大,而小于了乙物质的溶解度,即降温后甲析出的固体要多,所以此时甲溶液中溶质的质量分数要小于乙溶液中的溶质的质量分数,由于丙的溶解度随温度的降低而增大,所以虽然温度降低,但溶质和溶剂的质量不变,所以丙溶液的溶质的质量分数不会改变,但是仍然小于甲的溶解度,所以将三种饱和溶液分别从t2℃降温到t1℃时,所得溶液中溶质的质量分数由大到小的顺序为:乙>甲>丙。

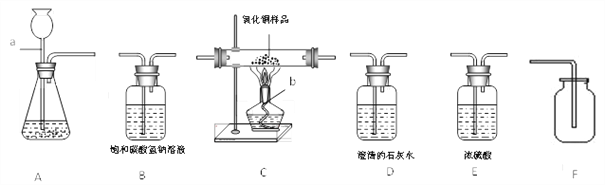
【题目】木炭还原氧化铜得到的红色固体是否全部是铜?
[查阅资料]
(1)铜有+1和+2价两种化合价;
(2)C也能将CuO还原为红色固体Cu2O ;
(3)Cu2O + H2SO4 ===== Cu + Cu SO4 + H2O ;
(4)Cu SO4溶液为蓝色。
[猜想] (1)红色固体只是Cu ;(2)红色固体只是Cu2O ;(3)红色固体是____________。
[实验探究]
实验操作 | 实验现象 | 实验结论 |
取3.6g红色固体放入烧杯中,向其中加入足量的稀硫酸充分反应后,静置。 | 若_______________ | 证明猜想(1)正确 |
若_______________ | 证明红色固体中肯定含有____________________ 可能含有_____________ |
为了进一步确定可能含有的物质是否存在,小华将反应后的液体过滤,将滤渣洗涤、干燥,称得其质量为3.5g ,根据上述数据判断猜想__________(填序号)正确。