题目内容
【题目】质量守恒定律是一条重要规律,请利用该定律的相关知识回答下列问题。
(1)化学反应前后肯定没有变化的是______(填序号)。
①原子数目②分子数目③元素种类④物质种类⑤原子种类⑥物质的总质量
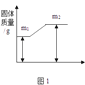
(2)镁条在空气中完全燃烧的化学方程式为_______(只考虑氧气参加反应,下同),若固体质量变化用图1表示,则m2与m1之差表示_______的质量。
(3)关于质量守恒定律,下列表述正确的是________。
A蜡烛燃烧后质量减少,说明质量守恒定律不是普遍规律
B每32gS和32gO2完全反应后,生成64gSO2
C在化学反应aA+bB→cC+dD中一定有:a+b=c+d
D 5g液态水完全蒸发可得到5g水蒸气,符合质量守恒定律
【答案】①③⑤⑥ 2Mg+O2![]() 2MgO 参加反应的氧气 B
2MgO 参加反应的氧气 B
【解析】
(1)化学变化一定符合质量守恒定律:化学反应前后肯定没有变化的是
①原子数目③元素种类⑤原子种类⑥物质的总质量
故选:①③⑤⑥
(2)镁条在空气中完全燃烧的化学方程式为:2Mg+O2![]() 2MgO,若固体质量变化用图1表示,则m2与m1之差表示参加反应的氧气质量。
2MgO,若固体质量变化用图1表示,则m2与m1之差表示参加反应的氧气质量。
(3)关于质量守恒定律,下列表述正确的是
A、蜡烛燃烧后质量减少,说明质量守恒定律不是普遍规律;故选项错误;
B、每32gS和32gO2完全反应后,生成64gSO2;故选项正确。
C、在化学反应aA+bB→cC+dD中一定有:a+b=c+d;故选项错误,
D、5g液态水完全蒸发可得到5g水蒸气,没有发生化学变化,不符合质量守恒定律;故选项错误。
故选:B。

【题目】化学兴趣小组的同学走进实验室制备并收集二氧化碳。同学们按下表进行实验,取等质量的大理石分别加入两种不同的酸中(杂质不与酸反应)进行三次实验,产生二氧化碳体积随时间变化曲线如图所示。
实验编号 | 药品 |
Ⅰ | 块状大理石、10% H2SO4溶液 |
Ⅱ | 块状大理石、7% HCl溶液 |
Ⅲ | 大理石粉末、7% HCl溶液 |

(1)图中丙曲线对应实验_______(选填“I”“Ⅱ”或“Ⅲ”)。
(2)小组的同学讨论确定用图中乙曲线对应的药品制备并收集二氧化碳,相应的符号表达式是______________;
(3)不用图中甲曲线对应的药品,理由是______________。