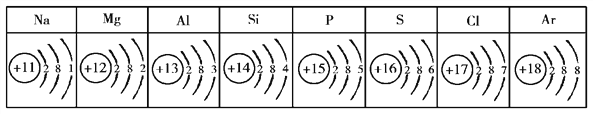
题目内容
【题目】经测定某氯化钠样品中混有硫酸钠,为了除去杂质并制得纯净的氯化钠固体,某同学设计方案如下:
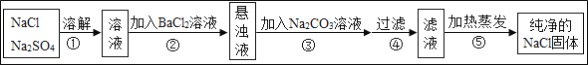
回答下列问题:
(1)操作②能否用硝酸钡溶液,并说明理由__________。
(2)此方案设计的是否严密,请说明理由______________。
【答案】不能,因为会引入新的杂质 NaNO3。不严密,过滤后滤液中存在 Na2CO3,需要加盐酸除去。
【解析】
(1)氯化钡和硫酸钠溶液反应会生成硫酸钡沉淀和氯化钠,反应的方程式为:BaCl2+Na2SO4═BaSO4↓+2NaCl;如操作②用硝酸钡溶液,则会生成硝酸钠引入新的杂质;(2)碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,所以操作③的目的是使钡离子完全沉淀;但是最后过量的碳酸钠没有除去,所以此设计方案不严密。

 名校课堂系列答案
名校课堂系列答案【题目】如图是电解水实验的示意图,回答下列问题:
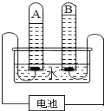
(1)写出该反应的化学方程式:_____。
(2)A 管接电池_____极(填“正”或“负”)。
(3)检验 B 试管中气体的操作方法和现象是_____。
(4)某学生观测记录了不同时间段A、B 试管内收集到的气体体积, 实验数据如下:
时间/分钟 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
A 试管气体体积(cm3) | 6 | 12 | 20 | 29 | 39 | 49 | 55 | 65 | 75 | 85 |
B 试管气体体积(cm3) | 2 | 4 | 7 | 11 | 16 | 21 | 26 | 31 | 36 | 41 |
仔细分析实验数据,1-4 min 内A、B 试管收集到的气体体积之比大于 2:1,可能的原因是____。
从第 8 分钟开始,每分钟内 A、B 试管收集的气体体积之比为 2:1,可能的原因是________。
(5)为进一步测定水中氢、氧元素质量比,某科技小组的同学设计了下列实验(装置如右图),通过称量反应前后装置 A、B 的质量,结果测得 m(H):m(O) >1:8,比理论值偏高,其原因可能是_____(填编号)。
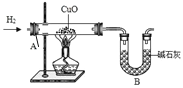
A.通入的氢气未经过净化干燥 B.装置 A 内管口有水凝结
C.氧化铜没有完全还原 D.装置B 同时吸收了空气中的水蒸气和CO2
【题目】联系所学的![]() 的性质,结合以下短文的相关信息,回答相关问题:
的性质,结合以下短文的相关信息,回答相关问题:
![]() 年,美国科学家卡尔克里斯特领导的研究小组成功地制取出盐粒大小的氮
年,美国科学家卡尔克里斯特领导的研究小组成功地制取出盐粒大小的氮![]() (化学式为
(化学式为![]() ).在制取氮
).在制取氮![]() 的实验中,它曾发生了爆炸,摧毁了实验室的部分设备.因此,科学家们认为,如果能让这种物质保持稳定;则它可能会成为火箭和导弹后级的理想燃料.氮
的实验中,它曾发生了爆炸,摧毁了实验室的部分设备.因此,科学家们认为,如果能让这种物质保持稳定;则它可能会成为火箭和导弹后级的理想燃料.氮![]() 是由排列成
是由排列成![]() 形的
形的![]() 个氮原子结合而成的,化学性质极不稳定.
个氮原子结合而成的,化学性质极不稳定.
![]() 比较氮气和氮
比较氮气和氮![]() 的异同点:
的异同点:
氮气 | 氮 | ||
不同点 | 分子构成 | ________ | ________ |
物理性质 | ________ | ________ | |
化学性质 | ________ | ________ | |
相同点 | _____________________________________ | ||
![]() 请你想象一下
请你想象一下![]() 在应用领域有哪些用途?(至少写
在应用领域有哪些用途?(至少写![]() 条)________,________.
条)________,________.
【题目】学习热情和学习方法是成才的必备条件,灵活掌握不同的学习方法可以取得事半功倍的效果.请用以下方法解决下列问题:
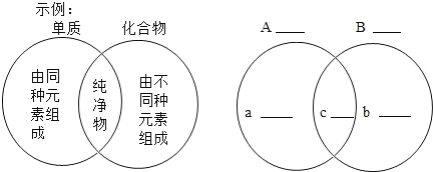
![]() 分类法:利用下列
分类法:利用下列![]() 组物质
组物质
![]() .
.![]() 、
、![]() 、
、![]() 、
、![]()
![]() .
.![]() 、
、![]() 、
、![]() 、
、![]()
![]() .金刚石与石墨的混合物、过氧化氢的水溶液、冰与水混合、氧气与臭氧混合
.金刚石与石墨的混合物、过氧化氢的水溶液、冰与水混合、氧气与臭氧混合
请按要求填写如表空白(填写物质的化学式或分类标准)
序号 |
|
|
|
分类标准 | 金属氧化物 | ________ | ________ |
属于该类别的物质 | ________ |
| ________ |
![]() 对比法:
对比法:
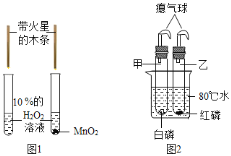
![]() .如图
.如图![]() 所示:其实验目的是探究________.
所示:其实验目的是探究________.
![]() .如图
.如图![]() 所示:杰克同学将盛有干燥白磷的甲试管和干燥红磷的乙试管插入盛有
所示:杰克同学将盛有干燥白磷的甲试管和干燥红磷的乙试管插入盛有![]() 的烧杯里(甲、乙试管均套有气球密封).过一会后,发现甲试管中的白磷燃烧,乙试管中的红磷没有燃烧.请根据杰克同学的实验现象,对比得出可燃物燃烧所需的条件之一:________.
的烧杯里(甲、乙试管均套有气球密封).过一会后,发现甲试管中的白磷燃烧,乙试管中的红磷没有燃烧.请根据杰克同学的实验现象,对比得出可燃物燃烧所需的条件之一:________.