题目内容
【题目】某化学活动小组以“酸、碱、盐的性质”为主题进行探究性学习,请你与他们一起解决下列问题。
(1)下面是该组同学在探究酸、碱、盐的性质时对某无色溶液所含溶质的记录,其中合理的是_____(填字母代号)。
a.氢氧化钠、碳酸钠、氯化钠
b.硝酸钾、氯化钠、氯化铁
c.氢氧化钙、碳酸钠、氯化钠
d.氢氧化钠、氯化钠、氯化氢
(2)我国化学家侯德榜发明了联合制碱法,所制得的“碱”的化学式是_____。
(3)通过查阅资料可知,过氧化钠固体(Na2O2)与水反应生成氢氧化钠和氧气,写出该反应的化学方程式_____。
(4)在学习NaOH性质时知道,氢氧化钠溶液久置在空气中易变质,如图是敞口放置的氢氧化钠溶液,康康同学想知道该溶液是否变质或变质的程度。
①写出氢氧化钠变质的原因。_____(用文字描述)
②请设计实验验证该溶液的成分。_____(简要写出实验步骤、现象和结论)
③如何除去少量变质的NaOH溶液中的杂质,用化学方程式表示_____。
(5)取部分变质的氢氧化钠溶液50g,向其中加入溶质质量分数为9.8%的稀硫酸50g.恰好完全反应得到中性溶液,计算反应后溶液中溶质的质量_____。
【答案】a Na2CO3 ![]() 氢氧化钠与空气中的二氧化碳反应生成碳酸钠而变质 取少量溶液,滴加过量的氯化钙(或氯化钡)溶液,若无明显现象,则没有变质,溶质成分为NaOH;若产生白色沉淀,则已变质,继续向溶液中滴加酚酞溶液,若溶液变红,则部分变质,溶质成分为Na2CO3、NaOH,若无明显现象,则全部变质,溶质成分为Na2CO3
氢氧化钠与空气中的二氧化碳反应生成碳酸钠而变质 取少量溶液,滴加过量的氯化钙(或氯化钡)溶液,若无明显现象,则没有变质,溶质成分为NaOH;若产生白色沉淀,则已变质,继续向溶液中滴加酚酞溶液,若溶液变红,则部分变质,溶质成分为Na2CO3、NaOH,若无明显现象,则全部变质,溶质成分为Na2CO3 ![]() (合理即可) 7.1g
(合理即可) 7.1g
【解析】
(1)a、氢氧化钠、碳酸钠、氯化钠能够共存,而且其水溶液呈无色。a正确;
b、硝酸钾、氯化钠、氯化铁能够共存,但是氯化铁的水溶液是黄色。b错误;
c、氢氧化钙、碳酸钠无法共存,会生成碳酸钙沉淀和氯化钠。c错误;
d、氢氧化钠和氯化氢无法共存,会生成氯化钠和水。d错误。
故选a;
(2)我国的“侯氏制碱法”制取的是纯碱,即碳酸钠。故答案为:Na2CO3;
(3)过氧化钠和水反应生成氢氧化钠和氧气。故答案为:![]() ;
;
(4)①氢氧化钠易吸收空气中的二氧化碳,与其反应生成碳酸钠和水,从而导致溶液变质。故答案为:氢氧化钠与空气中的二氧化碳反应生成碳酸钠而变质;
②检验该溶液中是否含有碳酸钠、氢氧化钠。可以先向溶液中加入氯化钙或氯化钡溶液,使其和碳酸钠反应生成沉淀,从而将碳酸钠除去。若此时溶液中溶质有氢氧化钠,则溶液呈碱性,可以滴加酚酞来确定溶液是否含有氢氧化钠。故答案为:取少量溶液,滴加过量的氯化钙(或氯化钡)溶液,若无明显现象,则没有变质,溶质成分为NaOH;若产生白色沉淀,则已变质,继续向溶液中滴加酚酞溶液,若溶液变红,则部分变质,溶质成分为Na2CO3、NaOH,若无明显现象,则全部变质,溶质成分为Na2CO3;
③氢氧化钠变质后转化为碳酸钠。即除去氢氧化钠的中的碳酸钠。应该选择一种物质与碳酸钠反应生成氢氧化钠,且该物质不和氢氧化钠反应。则该物质可以是氢氧化钙。氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠。该反应可以将碳酸钠除去,而不引入新的杂质。故答案为:![]() (合理即可);
(合理即可);
(5)解:消耗硫酸的质量为:50g×9.8%=4.9g。
设恰好完全反应生成硫酸钠的质量为x。
根据化学方程式:2NaOH+H2SO4=Na2SO4+2H2O和Na2CO3+H2SO4=Na2SO4+H2O+CO2↑可知:
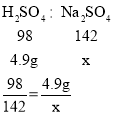
解得x=7.1g
答:反应后溶液中溶质的质量为7.1g。