题目内容
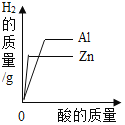
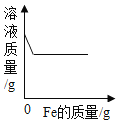
【题目】 工业盐酸中通常含少量FeC13而呈黄色,小亮为测定某工业盐酸中HCl的含量进行如下实验,取某工业盐酸50g,滴加溶质质量分数为20%的NaOH溶液,反应过程中,当加入的NaOH溶液质量至以下数值时,对充分反应后所得溶液的质量进行了测定,部分数据如下表,请根据表格和图象完成下列问题:
加入NaOH溶液的质量/g | 25 | 50 | 75 | 100 |
所得溶液的质量/g | 75 | 100 | 125 | m |

(1)开始没有产生沉淀的原因是_____。
(2)求该工业盐酸中HCl的质量分数______(写出计算过程)。
(3)m=_____(结果保留两位小数)
【答案】氢氧化钠先与盐酸反应 29.2% 148.93
【解析】
根据与盐酸反应的氢氧化钠的质量和对应的化学方程式求算该工业盐酸中HCl的质量分数,根据与氯化铁反应的氢氧化钠的质量和对应的化学方程式求算氢氧化铁的质量,进而求算m的数值。
(1)开始没有产生沉淀的原因是氢氧化钠先与盐酸反应。故填:氢氧化钠先与盐酸反应
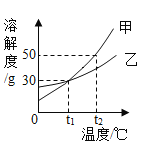
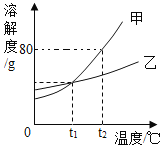
(2)根据图可知,与盐酸反应的氢氧化钠的溶液的质量为80g,设该工业盐酸中HCl的质量分数为x。
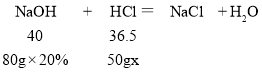
![]()
x=29.2%;故填:29.2%
(3)根据图可知,与氯化铁反应的氢氧化钠溶液的质量为6g,,设生成的氢氧化铁的质量为y。
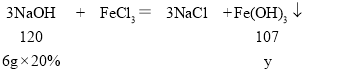
![]()
y=1.07g
m=50g+100g﹣1.07g=148.93g;故填:148.93

 名校课堂系列答案
名校课堂系列答案【题目】 为庆祝元素周期表诞生150周年,联合国将2019年定为国际化学元素周期表年,请根据下表(元素周期表的部分内容)完成下题:
周期/族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | 3 Li 锂 6.941 | 4 Be 铍 9.012 | 5B 硼 10.81 | 6C 碳 12.01 | 7N 氮 14.01 | 8O 氧 16.00 | 9F 氟 19.00 | 10Ne 氖 20.18 |
3 | 11Na 钠 22.99 | 12Mg 镁 24.31 | 13Al 铝 26.98 | 14Si 硅 28.09 | 15P 磷 30.97 | 16S 硫 32.06 | 17Cl 氯 35.45 | 18Ar 氩 39.95 |
Ⅰ.(1)请根据上表写出关于氩元素的一条信息:_____。
(2)镁与铝两种元素的最本质区别在于_____;由溴元素的原子结构示意图(如图所示)可知;溴元素与上表中的_____元素化学性质相似。
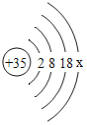
(3)第11号元素钠在化学反应中易_____(填“得到”或“失去”)电子。则钠元素和硫元素形成的化合物的化学式为_____。
(4)电池是高端电动汽车的主要动力源,其正极材料为LiCoO2,其中Co
Ⅱ.从化学视角看人体,人体就是一张元素周期表。
(1)“关爱生命,拥抱健康”是人类永恒的主题,下列说法不科学的是_____。
A只要患甲状腺肿大,就必须补充适量的碘
B适当晒太阳和增加维生素D的摄入,做到科学补钙
C人是大自然的一部分,人体中所含元素全部来自大自然
D低血糖病症发作时,喝葡萄糖水要比吃馒头见效快
(2)请根据生活常识结合已有知识胃酸的成份是盐酸而不是硫酸的原因_____。
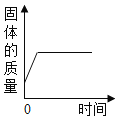
【题目】某同学为探究铁合金中铁的质量分数,先后进行了三次实验,实验数据如下表:
实验次数 项目 | 第一次 | 第二次 | 第三次 |
所取合金的质量/g | 20 | 20 | 40 |
所加稀硫酸的质量/g | 100 | 120 | 80 |
生成氢气的质量/g | 0.4 | 0.4 | 0.4 |
根据该同学的实验,试回答以下问题:
(1)上表三次实验中,合金里的铁恰好完全反应时,消耗稀硫酸溶液的质量是_____g.
(2)该铜铁合金中铁的质量分数是多少?_____。