题目内容
【题目】如图是化学实验中常用的几种装置。
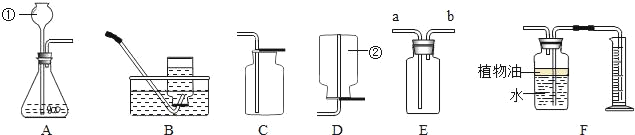
请回答下列问题:
(1)指出有编号的仪器名称:①_____,②_____。
(2)利用上述A、B装置的组合可以制取的一种常见气体,写出实验室制取该气体的化学反应方程式_____。
(3)若用E装置干燥生成的氧气,E中盛放的液体试剂是_____,气体应从_____端导入(填“a”或“b”)。
(4)F装置可用来测量生成的CO2气体的体积,其中在水面上放一层植物油的目的是_____,植物油上方原有的空气对实验的结果_____(填“有”或“没有”)明显影响。
(5)写出用石灰石和稀盐酸制取二氧化碳的化学方程式_____,可选用图中_____和_____(填标号)组装一套制取二氧化碳的装置。检验二氧化碳集满的方法是_____。
【答案】长颈漏斗 集气瓶 Zn+H2SO4=ZnSO4+H2↑或2H2O2![]() 2H2O+O2↑ 浓硫酸 a 防止二氧化碳溶于水 没有 CaCO3+2HCl═CaCl2+H2O+CO2↑ A C或E 将燃着的木条放于集气瓶口,若木条熄灭则满
2H2O+O2↑ 浓硫酸 a 防止二氧化碳溶于水 没有 CaCO3+2HCl═CaCl2+H2O+CO2↑ A C或E 将燃着的木条放于集气瓶口,若木条熄灭则满
【解析】
(1)图中所示的仪器名称为:①长颈漏斗;②集气瓶;
(2)A装置适合用于反应物是固体和液体,反应条件是常温,B装置适合于所收集的气体可以用排水法收集的;可以是实验室用双氧水制取氧气和利用锌和稀硫酸反应制取氢气,化学反应方程式为:Zn+H2SO4=ZnSO4+H2↑或2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
(3)浓硫酸具有吸水性,可以做干燥剂,E装置干燥生成的氧气时要长进短出;
(4)若要测二氧化碳的体积,可以将气体通过F装置,为了防止二氧化碳溶于水,所以在洗气瓶中添加了植物油,由于二氧化碳也会占据一定的体积,所以洗气瓶中的空气对实验结果几乎没有影响;
(5)大理石的主要成分为碳酸钙,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,其化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;该反应不需加热,属于固液常温型,故选发生装置A,二氧化碳的密度比空气大且能溶于水,最好用向上排空气法收集;检验二氧化碳是否收集满的方法是:用燃着的木条放于集气瓶口观察是否熄灭。

 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案【题目】我国西北地区有很多咸水湖,其中最大的是柴达木盆地的察尔汗盐池。某盐湖附近的农民通过“冬天捞碱,夏天晒盐”获得大量湖盐。小伟同学取该湖盐样品进行探究。
(提出问题)该湖盐样品的成分是什么?
(查阅资料)冬天捞碱的“碱”指Na2CO3,夏天晒盐的“盐”指NaCl。
(猜想与假设)猜想一:Na2CO3
猜想二:NaCl
猜想三:Na2CO3和NaCl
(实验探究)
实验 | 实验操作 | 实验现象 | 实验结论 |
实验一 | 取少量样品于试管中,加适量水溶解后,加入过量稀HNO3 | 产生能使澄清石灰水变浑浊的气体 | ①猜想_____不成立 |
实验二 | ②向实验一所得的溶液中加入适量的_____ | ③_____ | 猜想三成立 |
(拓展延伸)为进一步确定该湖盐样品中Na2CO3的质量分数,小伟同学再取该湖盐样品10.00g做了如图1所示的补充实验。
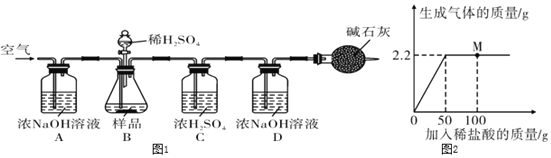
(1)反应结束之后通入空气的目的是_____。
(2)装置A中浓NaOH溶液的作用是_____(用方程式表示)。
(3)实验结束后测得装置D增重0.44g,则湖盐样品中Na2CO3的质量分数为_____%(保留一位小数)。
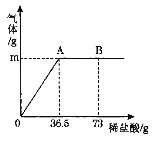
(4)向6g氯化钠和碳酸钠的固体混合物中不断加入稀盐酸,发生反应的化学方程式为Na2CO3+2HCl═2NaCl+H2O+CO2↑,反应过程中生成气体的质量与加入稀盐酸的质量关系如图2所示。求:
①恰好完全反应时,生成气体的质量为_____。
②M点所对应的溶液中的溶质有_____(填化学式)。
③恰好完全反应时,所得溶液中溶质的质量分数_____。