题目内容
【题目】下图是在一定量氢氧化钠溶液中不断加入盐酸的曲线图,纵坐标能表示的意义是( )
A.氢氧化钠的质量
B.生成氯化钠的质量
C.溶液中水的质量
D.溶液的pH值
【答案】B
【解析】A、氢氧化钠和盐酸反应生成了氯化钠,消耗氢氧化钠的质量,质量减少,A不符合题意;
B、氢氧化钠和盐酸反应生成了氯化钠,所以开始加入稀盐酸时即产生氯化钠,等把氢氧化钠消耗完全后氯化钠的质量不再增加,故B符合题意;
C、由于盐酸中含有水,所以不管反应是否完全,水的质量是随着盐酸的加入而不断增加的,故C不符合题意;
D、溶液的pH值逐渐减少,D不符合题意.
所以答案是:B.
【考点精析】本题主要考查了中和反应及其应用的相关知识点,需要掌握中和反应:酸与碱作用生成盐和水的反应才能正确解答此题.

 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案【题目】同学们查阅资料,镁是一种化学性质非常活泼的金属,可以在多种气体中燃烧。同学们用下图所示装置分别进行镁条在二氧化碳和氮气中燃烧的实验。B中观察到镁冒出淡黄色的烟,并闻到刺激性气味。同学们对两个反应进行了探究。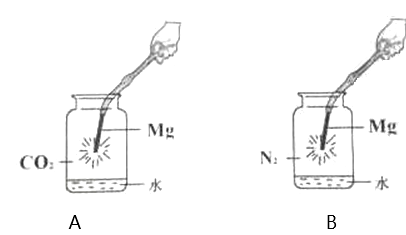
[查阅资料]
①氧化镁、碳酸镁均可以和盐酸反应。
②氮化镁(Mg3N2),淡黄色固体,无味,遇水产生白色沉淀氢氧化镁,并产生有刺激
性气味的氨气(NH3)。
实验1探究A中生成黑色固体和白烟的成分。
(1)[猜想与假设]1、黑色固体是炭。2、白烟可能是MgO 、MgCO3或
(2)[进行实验]
实验操作 | 实验现象 | 实验结论 |
①取A中生成的固体于试管中,加入适量稀盐酸 | 白色固体消失,无气泡生成。 | 。 |
②将①反应后的剩余物过滤,将滤渣洗涤干燥后在盛有氧气的集气瓶中点燃,熄灭后,向瓶中倒入澄清石灰水 | 黑色固体燃烧,发白光,放热,澄清石灰水变浑浊。 | 黑色固体是炭。 |
实验2 探究B中闻到刺激性气味的原因。
同学们根据查阅的资料分析,镁条在氮气中燃烧闻到刺激性气味的原因与集气瓶中的水有关。请你在已有实验的基础上,设计一个实验方案证明同学们的猜想正确。
(3)[反思与评价]
通过探究,同学们对燃烧和灭火有了新的认识。
