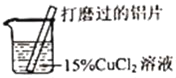题目内容
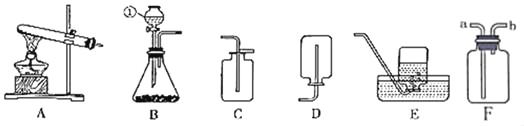
【题目】根据下列装置图,回答有关问题。

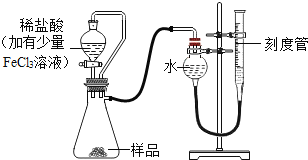
(1)写出图中标号仪器的名称:a_____。
(2)实验室可用氯酸钾和二氧化锰制取氧气,化学方程式为_____。
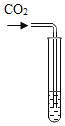
(3)实验室可用F装置代替B制取二氧化碳,铜丝网上应放置的药品是_____,反应的化学方程式为_____,可选用的收集装置是_____(填字母)。
(4) 实验室可用锌和稀硫酸制取氢气,6.5g锌与足量稀硫酸反应,最多可生成氢气的质量是多少?_____(写出计算过程)
【答案】长颈漏斗 2KClO3 2KCl+3O2↑ 石灰石(或大理石) CaCO3+2HCl=CaCl2+CO2↑+H2O D 0.2g
2KCl+3O2↑ 石灰石(或大理石) CaCO3+2HCl=CaCl2+CO2↑+H2O D 0.2g
【解析】
(1)仪器a的名称是长颈漏斗;
(2)氯酸钾和二氧化锰在加热下生成氯化钾和氧气,反应的化学方程式为2KClO3 2KCl+3O2↑;
2KCl+3O2↑;
(3)实验室用石灰石(或大理石)和稀盐酸反应制取二氧化碳,若用F装置代替B制取二氧化碳,则铜丝网上应放置的药品是石灰石(或大理石);
碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O;
二氧化碳能与水反应,且密度比空气大,故选用向上排空气法收集,收集装置选用D;
(4)设最多产生氢气的质量为x,计算过程如下: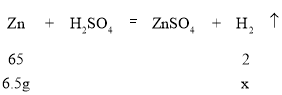
![]() ,解得x=0.2g,故最多产生氢气的质量为0.2g。
,解得x=0.2g,故最多产生氢气的质量为0.2g。

【题目】某化学兴趣小组的同学在实验室对铝与氯化铜溶液的反应进行了如下探究,请回答相关问题。
实验操作 | 实验现象 |
| ①有红色物质附着于铝片表面 ②铝片表面逸出大量无色气体,放出大量的热 ③烧杯底部出现红色沉淀和白色沉淀 |
(1)打磨铝片的目的是_____。
(2)现象①③的红色物质为铜,生成铜的化学方程式为_____。
(3)收集逸出的无色气体,经检验具有可燃性,该气体为_____(写化学式),说明氯化铜溶液显_____性。
(查阅资料)氯化亚铜(CuC1)是一种微溶于水的白色固体,在空气中易被氧化成褐色的Cu(OH)Cl。
(4)取杯底的白色沉淀暴露在空气中,一段时间后观察到变成褐色,说明白色物质为氯化亚铜。该变色反应的产物只有 Cu(OH)Cl,反应的化学方程式为_____。
(发现问题)氯化亚铜的生成与反应条件有关吗?
(提出猜想)猜想I:与反应物的浓度有关;猜想Ⅱ:与反应的_____有关。
(实验探究)
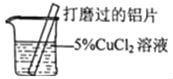
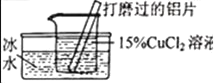
实验设计 |
|
|
实验现象 | 有红色沉淀和无色气体生成,无白色沉淀生成。 | 有红色沉淀和无色气体生成,_____ |
实验结论 | 猜想I成立 | 猜想Ⅱ成立 |
(拓展与思考)氯化亚铜是否是反应生成的铜与溶液中的氯化铜发生 Cu+CuCl2=2CuCl反应生成的?可用试管取15%的氯化铜溶液,向其中加入_____并加热的方法来验证。
【题目】某化学课堂进行“酸碱中和反应”实验,请你和他们一起完成实验探究。
[实验]将一定量稀盐酸加入到盛氢氧化钙溶液的小烧杯中。该反应的化学方程式是_______________。
[查阅资料]CaC12溶液显中性,Ca(OH)2溶液显碱性的原因是溶液含有_____________(用微粒符号表示)。
[提出问题]部分同学产生了疑问:反应后溶液中溶质的成分是什么?
[猜想与假设]针对疑问,甲组同学猜想如下:
猜想I:只有CaC12
猜想II:有_____________
猜想III:有CaCl2和Ca(OH)2
猜想IV:有CaCl2、HCl和Ca (OH)2
乙组同学对以上猜想提出质疑,认为猜想IV不合理,其理由是________________。
[实验探究]为了验证其余猜想,各小组进行了下列三个方案的探究。
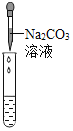
实验方案 | 滴加酚酞溶液 | 通入CO2 | 滴加Na2CO3溶液 |
实验操作 |
|
|
|
实验现象 | _____________ | _____________ | 产生白色沉淀 |
实验结论 | 溶液中含有Ca (OH)2 | 溶液中含有Ca (OH)2 | 溶液中含有Ca (OH)2 |
[得出结论]通过探究,全班同学一致确定猜想III是正确的。
[评价反思](1)丙组同学认为滴加Na2CO3溶液产生白色沉淀,并不能证明溶液中一定含有Ca(OH)2,请你帮助他们说明原因___________________。
(2)在分析反应后所得溶液中溶质的成分时,除了考虑生成物外,还需要考虑_____________。