题目内容
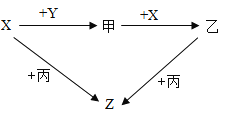
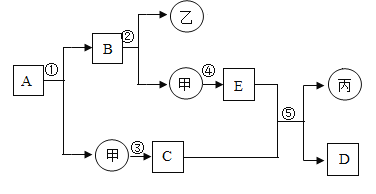
【题目】如图是初中化学常见物质间的转化关系,其中甲、乙、丙为单质:A、B、C、D、E为化合物,且A与B的组成元素相同,D与E的组成元素也相同。己知D能使澄清的石灰水变浑浊,反应③的现象是火星四射,生成黑色固体。反应条件、部分反应物和生成物已略去。
(1)写出反应①的化学方程式_____
(2)写出D物质的一种用途_____
(3)写出生成物乙与甲的体积比(相同状况下)_____
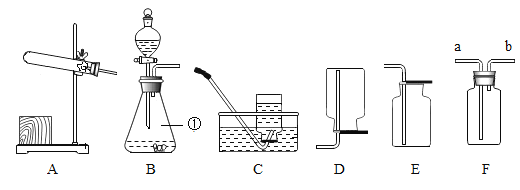
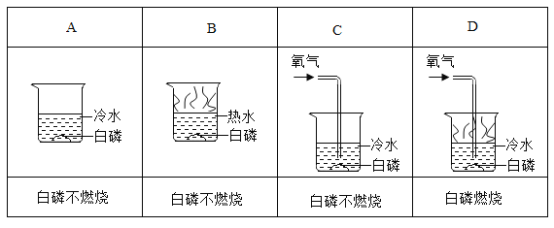
(4)反应③进行过程中集气瓶底部需放入_____
(5)E具有毒性的原因_____
(6)写出反应⑤的化学方程式_____此反应中,_____具有还原性(填图中符号)。
【答案】2H2O2![]() 2H2O+ O2↑ 灭火等(合理即可) 2:1 少量的水或细砂 一氧化碳与血液中的血红蛋白结合,使人体缺氧而死亡; Fe3O4+4CO
2H2O+ O2↑ 灭火等(合理即可) 2:1 少量的水或细砂 一氧化碳与血液中的血红蛋白结合,使人体缺氧而死亡; Fe3O4+4CO![]() 3Fe+4CO2 E
3Fe+4CO2 E
【解析】
A能生成B和单质甲,且A与B的组成元素相同,过氧化氢在二氧化锰催化作用下分解生成水和氧气,可判断A可能为过氧化氢、B为水; B又能生成单质甲和乙,水在通电时生成氢气和氧气,即可确定B为水,甲为氧气,乙为氢气;反应③的现象是火星四射,生成黑色固体,铁在氧气中燃烧火星四射,生成黑色固体四氧化三铁,故C为四氧化三铁;D能使澄清的石灰水变浑浊,则D是二氧化碳,E、D组成元素相同,E则是一氧化碳,C和E在高温条件下反应可生成丙和D,进一步证明了E和D分别是一氧化碳和二氧化碳,带入框图,推断合理。
根据以上分析可知:
(1)反应①是过氧化氢在二氧化锰催化作用下分解生成水和氧气,反应的化学方程式为:2H2O2![]() 2H2O+ O2↑;
2H2O+ O2↑;
(2)D物质是二氧化碳,可用作灭火等;
(3)水在通电时生成氢气和氧气,反应的化学方程式为:2H2O ![]() 2H2↑+ O2 ↑,根据化学方程式可知,生成物乙与甲的体积比(相同状况下)=2:1;
2H2↑+ O2 ↑,根据化学方程式可知,生成物乙与甲的体积比(相同状况下)=2:1;
(4)反应③是铁在氧气中燃烧,该反应放出大量的热,生成物的温度较高,溅落瓶底会引起集气瓶的炸裂,所以进行过程中集气瓶底部需放入少量的水或细砂;
(5)E是一氧化碳,具有毒性的原因一氧化碳与血液中的血红蛋白结合,使人体缺氧而死亡;
(6)反应⑤是四氧化三铁与一氧化碳在高温条件下反应生成铁和二氧化碳,反应的化学方程式为:Fe3O4+4CO![]() 3Fe+4CO2;此反应中, E在反应中得到氧元素,具有还原性。
3Fe+4CO2;此反应中, E在反应中得到氧元素,具有还原性。