题目内容
(1)氧化物 RO 中含氧元素的质量分数为 40%,则 R 元素的相对原子质量为 ;
(2)人吸烟时会吸入一种有毒气体,这种气体中只含碳、氧两种元素,且元素质量比为3:4,则该气体的化学式为 ,其中碳元素的化合价为 .
(2)人吸烟时会吸入一种有毒气体,这种气体中只含碳、氧两种元素,且元素质量比为3:4,则该气体的化学式为
分析:(1)根据化合物中元素的质量分数=
×100%,进行分析解答.
(2)根据题意,人吸烟时会吸入一种有毒气体,这种气体中只含碳、氧两种元素,且元素质量比为3:4,由化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
| 相对原子质量×原子个数 |
| 相对分子质量 |
(2)根据题意,人吸烟时会吸入一种有毒气体,这种气体中只含碳、氧两种元素,且元素质量比为3:4,由化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
解答:解:(1)氧化物 RO中含氧元素的质量分数为 40%,设R元素的相对原子质量为x,则
×100%=40% x=24.
(2)根据题意,人吸烟时会吸入一种有毒气体,这种气体中只含碳、氧两种元素,且元素质量比为3:4;设该氧化物的化学式为CxOy,则12x:16y=3:4,x:y=11,则该气体的化学式为CO;氧元素显-2价,设碳元素的化合价是z,根据在化合物中正负化合价代数和为零,可得:x+(-2)=0,则z=+2价.
故答案为:(1)24;(2)CO;+2.
| x |
| x+16 |
(2)根据题意,人吸烟时会吸入一种有毒气体,这种气体中只含碳、氧两种元素,且元素质量比为3:4;设该氧化物的化学式为CxOy,则12x:16y=3:4,x:y=11,则该气体的化学式为CO;氧元素显-2价,设碳元素的化合价是z,根据在化合物中正负化合价代数和为零,可得:x+(-2)=0,则z=+2价.
故答案为:(1)24;(2)CO;+2.
点评:本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案
相关题目
还原某金属R的氧化物2.32克,可得到金属1.68克.若已知金属R的相对原子质量为56,则此金属氧化物化学式为( )
| A、R2O3 | B、R3O4 | C、RO2 | D、RO |
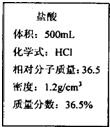 现有一瓶浓盐酸,标签如图所示,请根据标签上的数据回答问题:
现有一瓶浓盐酸,标签如图所示,请根据标签上的数据回答问题: