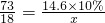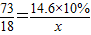题目内容
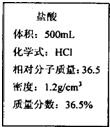 现有一瓶浓盐酸,标签如图所示,请根据标签上的数据回答问题:
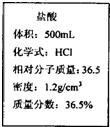
现有一瓶浓盐酸,标签如图所示,请根据标签上的数据回答问题:(1)取用8mL如右图所示标签的浓盐酸可以配制溶质质量分数为10%的稀盐酸的质量为
(2)利用刚配制的稀盐酸来测定某金属氧化物的化学式:取1.6g该金属氧化物(RO),向其中滴入刚配好的稀盐酸至恰好完全反应,共用去稀盐酸14.6g.
①写出发生反应的化学方程式
②利用已知条件求解生成水质量(x)的比例式
| 73 |
| 18 |
| 14.6×10% |
| x |
③金属氧化物的化学式是
④若向反应后溶液中加入118.8g水后,此时所得溶液中溶质的质量分数为
分析:(1)先根据公式m=ρv计算出所给8mL盐酸的质量,再根据溶液稀释前后溶质质量不变的原则即可求解;
(2)①书写方程式时要注意R的化合价;
②③根据化学方程式的计算可得出答案;
④反应后的溶液为氯化铜溶液,溶质氯化铜的质量可根据化学方程式计算,溶液总质量为化学反应中生成的溶液质量+产生水的质量.
(2)①书写方程式时要注意R的化合价;
②③根据化学方程式的计算可得出答案;
④反应后的溶液为氯化铜溶液,溶质氯化铜的质量可根据化学方程式计算,溶液总质量为化学反应中生成的溶液质量+产生水的质量.
解答:解:(1)先根据公式m=ρv计算出所给8mL盐酸的质量=1.2g/cm3×8mL=9.6g
再根据溶液稀释前后溶质质量不变即:稀释前溶液质量×稀释前溶质质量分数=稀释后溶液质量×稀释后溶质质量分数,
设需10%的盐酸质量为y,
根据:稀释前溶液质量×稀释前溶质质量分数=稀释后溶液质量×稀释后溶质质量分数可知:9.6×36.5%=10%y
解得:y=35
稀盐酸配制过程中用到的实验仪器为:胶头滴管、烧杯、玻璃棒和量筒可知,答案为:量筒
故答案为:35 量筒
(2)①、书写方程式时根据R的化合价为+2,可得方程式为:RO+2HCl=H2O+RCl2
故答案为:RO+2HCl=H2O+RCl2
②、由①可知:化学方程式为:
RO+2HCl=H2O+RCl2
73 18
14.6×10% x
可得:
=
故答案为:
=
③、设R的相对原子质量为a,根据化学方程式:
RO+2HCl=H2O+RCl2
a+16 73
1.6 14.6×10%
可得:
=
解得:a=64
可知R为铜
故选CuO
④、由③可知,R为铜,故化学方程式为:CuO+2HCl=H2O+CuCl2
设生成CuCl2为b
CuO+2HCl=H2O+CuCl2
73 135
14.6×10% b
可得:
=
∴b=2.7
根据质量守恒定律 生成氯化铜溶液的质量=氧化铜质量+盐酸质量=1.6+14.6=16.2
所以添加水后氯化铜溶液的总质量=16.2+118.8=135
所以氯化铜溶液中溶质质量分数=
×100%=
×100%=2%
故答案为:2%
再根据溶液稀释前后溶质质量不变即:稀释前溶液质量×稀释前溶质质量分数=稀释后溶液质量×稀释后溶质质量分数,
设需10%的盐酸质量为y,
根据:稀释前溶液质量×稀释前溶质质量分数=稀释后溶液质量×稀释后溶质质量分数可知:9.6×36.5%=10%y
解得:y=35
稀盐酸配制过程中用到的实验仪器为:胶头滴管、烧杯、玻璃棒和量筒可知,答案为:量筒
故答案为:35 量筒
(2)①、书写方程式时根据R的化合价为+2,可得方程式为:RO+2HCl=H2O+RCl2
故答案为:RO+2HCl=H2O+RCl2
②、由①可知:化学方程式为:
RO+2HCl=H2O+RCl2
73 18
14.6×10% x
可得:
| 73 |
| 18 |
| 14.6×10% |
| x |
故答案为:
| 73 |
| 18 |
| 14.6×10% |
| x |
③、设R的相对原子质量为a,根据化学方程式:
RO+2HCl=H2O+RCl2
a+16 73
1.6 14.6×10%
可得:
| a+16 |
| 73 |
| 1.6 |
| 14.6×10% |
解得:a=64
可知R为铜
故选CuO
④、由③可知,R为铜,故化学方程式为:CuO+2HCl=H2O+CuCl2
设生成CuCl2为b
CuO+2HCl=H2O+CuCl2
73 135
14.6×10% b
可得:
| 73 |
| 135 |
| 14.6×10% |
| b |
∴b=2.7
根据质量守恒定律 生成氯化铜溶液的质量=氧化铜质量+盐酸质量=1.6+14.6=16.2
所以添加水后氯化铜溶液的总质量=16.2+118.8=135
所以氯化铜溶液中溶质质量分数=
| 氯化铜质量 |
| 溶液总质量 |
| 2.7 |
| 135 |
故答案为:2%
点评:本题考查有关化学方程式的简单计算.

练习册系列答案
相关题目
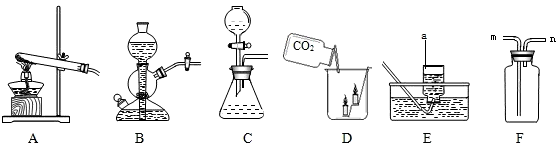
(2010?宝山区一模)下图是实验室常用的实验装置:
据此回答下列问题:
(1)写出a 仪器的名称
(2)①若实验室用B装置制取二氧化碳气体,则制取气体的原料可选用
A.稀硫酸和块状大理石 B.浓盐酸和块状大理石
C.稀盐酸和粉末状大理石 D.稀盐酸和块状大理石
②实验室制取二氧化碳的化学方程式是:
③实验室要配制一定质量的稀盐酸制取二氧化碳,现有一瓶浓盐酸,标签如下图所示.欲将该瓶浓盐酸完全稀释成10%的稀盐酸,需要加水的质量是

据此回答下列问题:
(1)写出a 仪器的名称
集气瓶
集气瓶
,B套发生装置的名称:启普发生器
启普发生器
,使用B发生装置的优点是便于添加液体药品,随时可使反应发生或停止
便于添加液体药品,随时可使反应发生或停止
.(2)①若实验室用B装置制取二氧化碳气体,则制取气体的原料可选用
D
D
.A.稀硫酸和块状大理石 B.浓盐酸和块状大理石
C.稀盐酸和粉末状大理石 D.稀盐酸和块状大理石
②实验室制取二氧化碳的化学方程式是:
CaCO3+2HCl═CaCl2+H2O+CO2↑
CaCO3+2HCl═CaCl2+H2O+CO2↑
.③实验室要配制一定质量的稀盐酸制取二氧化碳,现有一瓶浓盐酸,标签如下图所示.欲将该瓶浓盐酸完全稀释成10%的稀盐酸,需要加水的质量是
1593
1593
克.
| 化学纯 盐酸 含HCl 37% 密度 1.18g.cm-3 容量 500mL XX化学试剂厂(3)若用F装置收集二氧化碳,则气体应从 m m 端(填m或n)进入;若将收集到的二氧化碳气体沿烧杯壁倒入D(蜡烛已点燃)中,出现的现象是下面的蜡烛先灭,上面的蜡烛后灭 下面的蜡烛先灭,上面的蜡烛后灭 ,该实验说明二氧化碳具有不燃烧,也不支持燃烧,密度比空气大 不燃烧,也不支持燃烧,密度比空气大 的性质.(4)实验室用装置A、C均能制取氧气,这两种方法中,最能体现“节能环保”理念的是(用化学方程式): 2H2O2
2H2O2 ,该反应中二氧化锰的作用是
催化剂 催化剂 ;实验室用装置E收集的氧气不纯,可能产生的原因是集气瓶中没有装满水,混有空气 集气瓶中没有装满水,混有空气 .
下图是实验室常用的实验装置: |
| 化学纯 盐酸 含HCl 37% 密度 1.18g.cm-3 容量 500mL XX化学试剂厂 |
(4)实验室用装置A、C均能制取氧气,这两种方法中,最能体现“节能环保”理念的是(用化学方程式):________,该反应中二氧化锰的作用是________;实验室用装置E收集的氧气不纯,可能产生的原因是________.
 现有一瓶浓盐酸,标签如图所示,请根据标签上的数据回答问题:
现有一瓶浓盐酸,标签如图所示,请根据标签上的数据回答问题: