题目内容
【题目】碘元素(元素符号为I)的原子结构示意图为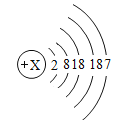 ,请回答下列问题。
,请回答下列问题。
(1)x的值为___。
(2)“加碘食盐”中一般加入碘酸钾(化学式为KIO3),这里的“碘”指的是___(填原子或元素)碘元素化合价为_____。
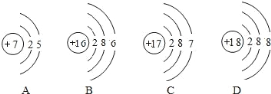
(3)一般情况下,元素原子的最外层电子数相同,具有相似的化学性质。碘元素的化学性质与图中元素的化学性质最相似的是___(填序号)。
【答案】53 元素 +5 C
【解析】
(1)根据原子结构示意图,圈内的数字表示核内质子数;在原子中,原子序数=质子数=核电荷数=核外电子数,可得 x的值为 2+8+18+18+7=53;
(2)物质由元素组成,“加碘食盐”中一般加入碘酸钾(化学式为KIO3),这里的“碘”指的元素;根据在化合物中正负化合价代数和为零,可得KIO3中碘元素化合价为(+1)+y+(-2)×3=0;y=+5;
(3)根据题意元素原子的最外层电子数相同,具有相似的化学性质,观察结构示意图,可得碘元素的化学性质与C元素的化学性质最相似。

 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案【题目】某兴趣小组对氯酸钾分解反应的催化剂进行研究,在相同的加热条件下,用如图装置完成表中实验:
编号 | 氯酸钾质量/g | 催化剂 | 催化剂质量/g | 收集50mL氧气所需时间/s |
实验1 | 5 | - | - | 171 |
实验2 | 5 | 二氧化锰 | 0.5 | 49 |
实验3 | 5 | 氧化铁 | 0.5 | 58 |
实验4 | 5 | 氯化钾 | 0.5 | 154 |
(1)设置实验1的目的是______________;
(2)表中所列3种催化剂的催化效果最佳的是_________________;
(3)写出氯酸钾分解的化学方程式:__________________;
(4)由实验1和实验4可知,氯化钾有_________________(填“有”或“无”)催化作用。维持加热条件不变,用实验1再继续收集50mL氧气,所需时间明显少于171s,解释原因:______________;
(5)要比较氯酸钾分解反应中不同催化剂的催化效果,除了测量收集50mL氧气所需时间外,还可以______________。
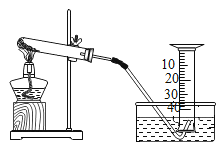
(拓展探究)同种催化剂,还有哪些因素会影响氯酸钾分解反应的催化效果?
假设: _________________________。
方案: _______________________。
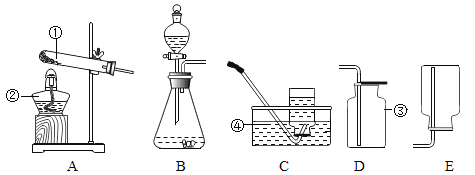
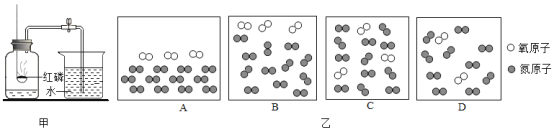
【题目】(一) 下图所示为实验室中常见的气体制备和收集装置.
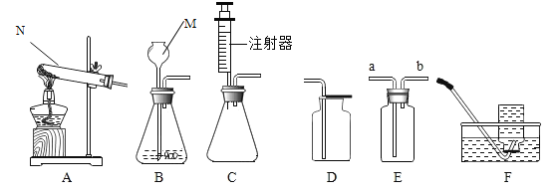
请回答下列问题:
(1)实验室用高锰酸钾制取氧气,应选用的发生装置是_____ (填字 母序号)。若用装置B制取二氧化碳,反应的原理是(用化学方程式表示)_____。
(2)实验室用H2O2溶液和MnO2制取氧气, 若选用C做发生装置,你认为选用C的优点是_____。
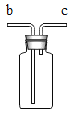
(3)欲使用装置E用排空气法收集二氧化碳,则气体应从_____ (填“a”或“b”) 端通入:欲使用装置E.用排水法收集氧气,先将瓶中装满水,再将气体从_____ (填“a”或“b”) 端通入。
(4)已知一氧化氮气体难落于水,在空气中容易与氧气发生反应,则收集一氧化氮气体时应选用图中装置_____(填字母序号)。
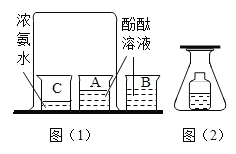
(二)小红同学进行酸碱中和反应的实验(如图所示)。她向氢氧化钠溶液中滴加一定量稀盐酸后,想起氢氧化钠溶液中事先没有滴加指示剂,为了确定盐酸与氢氧化钠的反应程度,她从烧杯中取了少量溶液于试管中,井向试管中滴加几滴无色酚酞试液,振荡,观察到试管中溶液颜色没有变化。于是她对烧杯中的溶液进行了以下探究:
(1)小红认为此时烧杯中的溶液可能有以下三种情况:
①盐酸与氢氧化钠恰好完全反应:②氢氧化钠有剩余:③盐酸过量。
小明同学却断定不可能“氢氧化钠有剩余”,他的理由是:_____。
(2)他们共同设计了一个实验方案,欲对上述其他两种可能情况进行验证。请根据相关内容填写如表:
实验方法 | 可能观察到的现象 | 结论 |
将少量锌粒放入试管中,然后从烧杯中取适量溶液至试管中。 | 如果_____。 | 则盐酸过量 |
如果_____。 | 则盐酸与氢氧化钠恰好完全反应 |
(3)经过讨论,他们认为利用下列几种物质代替锌粒,也可以达到验证目的。你认为其中不正确的是_____。(填序号).
A 生锈的铁钉
B 碳酸钠粉末
C 硫酸钠粉末
D 氢氧化铜
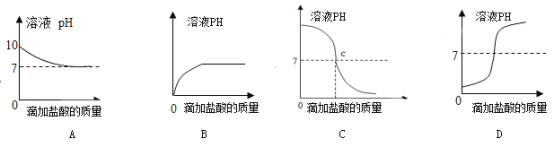
(4)如图曲线能够表示小红所做试验中溶液pH变化趋势的是_____(填序号)。