题目内容
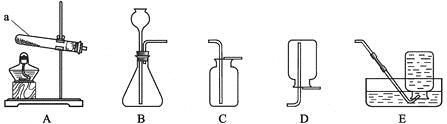
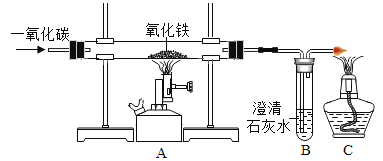
【题目】某兴趣小组对氯酸钾分解反应的催化剂进行研究,在相同的加热条件下,用如图装置完成表中实验:
编号 | 氯酸钾质量/g | 催化剂 | 催化剂质量/g | 收集50mL氧气所需时间/s |
实验1 | 5 | - | - | 171 |
实验2 | 5 | 二氧化锰 | 0.5 | 49 |
实验3 | 5 | 氧化铁 | 0.5 | 58 |
实验4 | 5 | 氯化钾 | 0.5 | 154 |
(1)设置实验1的目的是______________;
(2)表中所列3种催化剂的催化效果最佳的是_________________;
(3)写出氯酸钾分解的化学方程式:__________________;
(4)由实验1和实验4可知,氯化钾有_________________(填“有”或“无”)催化作用。维持加热条件不变,用实验1再继续收集50mL氧气,所需时间明显少于171s,解释原因:______________;
(5)要比较氯酸钾分解反应中不同催化剂的催化效果,除了测量收集50mL氧气所需时间外,还可以______________。
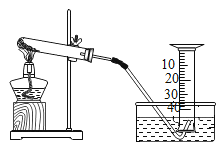
(拓展探究)同种催化剂,还有哪些因素会影响氯酸钾分解反应的催化效果?
假设: _________________________。
方案: _______________________。
【答案】对照实验 二氧化锰 2KClO3![]() 2KCl+3O2↑ 有 生成的KCl加快了反应速率 测量相同时间内收集气体的体积 同种催化剂,催化剂的颗粒大小不同,催化效果不同 将相同质量的氯酸钾与不同颗粒大小质量相同的同种催化剂充分混合,分别加热,测定收集50mL氧气所需时间
2KCl+3O2↑ 有 生成的KCl加快了反应速率 测量相同时间内收集气体的体积 同种催化剂,催化剂的颗粒大小不同,催化效果不同 将相同质量的氯酸钾与不同颗粒大小质量相同的同种催化剂充分混合,分别加热,测定收集50mL氧气所需时间
【解析】
氯酸钾和二氧化锰加热生成氯化钾和氧气。
(1)实验1没有催化剂,故设置实验1的目的是对照实验。
(2)实验2加入二氧化锰,收集50 mL氧气所需时间最短,故表中所列3种催化剂的催化效果最佳的是二氧化锰。
(3)氯酸钾和二氧化锰加热生成氯化钾和氧气,氯酸钾分解的化学方程式为2KClO3![]() 2KCl+3O2↑。
2KCl+3O2↑。
(4)由实验1和实验4可知,实验4中加入氯化钾,收集50 mL氧气所需时间缩短,故氯化钾有催化作用。维持加热条件不变,用实验1再继续收集50mL 氧气,所需时间明显少于171s,解释原因生成的KCl加快了反应速率。
(5)要比较氯酸钾分解反应中不同催化剂的催化效果,除了测量收集50 mL 氧气所需时间外,还可以测量相同时间内收集气体的体积。
[拓展探究]
假设:同种催化剂,催化剂的颗粒大小不同,催化效果不同。
方案:将相同质量的氯酸钾与不同颗粒大小质量相同的同种催化剂充分混合,分别加热,测定收集50mL氧气所需时间。

 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案【题目】在一定条件下,在一个密闭容器内发生某反应,测得反应过程中各物质的质量如下表所示,下列说法错误的是
物质 | a | b | c | d |
反应前质量(g) | 10 | 10 | 10 | 2 |
反应后质量(g) | 待测 | 2 | 21 | 2 |
A.该反应是化合反应,d可能是催化剂
B.a、b两种物质中元素种类一定与c物质中元素种类相同
C.b物质可能是单质
D.反应后a物质的质量为3g