题目内容
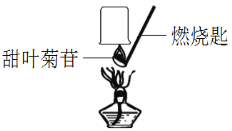
【题目】甜叶菊苷具有高甜度低热能的特点,是一种新型甜味剂,我国是全球最主要的生产国。小晴同学取适量的甜叶菊苷按图进行操作,并分别将干冷的烧杯和蘸有澄清石灰水的烧杯倒置于火焰上方。观察到_______和澄清石灰水变浑浊,由此确定甜叶菊苷中一定含有碳、氢元素。
为了进一步确定其元素组成,利用下图进行实验。(已知:①装置C中的氧化铜能确保甜叶菊苷中的碳元素完全转化为二氧化碳②氢氧化钠可以与二氧化碳反应)
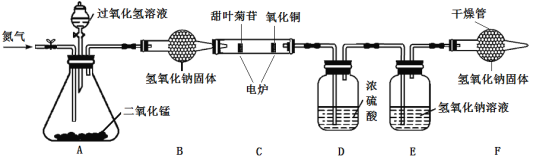
(1)实验前要通一会儿氮气,目的是________。
(2)A装置中发生反应的化学方程式为________。
(3)4.02g甜叶菊苷在C装置中充分燃烧后,D装置增重2.7g,E装置增重8.36g。(产物被完全吸收)数据分析:4.02g甜叶菊苷中氧元素的质量为____g,由此可以确定甜叶菊苷是由碳、氢、氧元素组成。
(4)若没有F装置,对氧元素质量测定结果的影响是____(填“偏大”、“偏小”或“无影响”)。
【答案】干冷的烧杯内壁出现水雾 排出装置内的空气 2H2O2 ![]() 2H2O+O2
2H2O+O2![]() 1.44 g 偏小
1.44 g 偏小
【解析】
若甜叶菊苷中含有氢元素,甜叶菊苷燃烧时会产生水蒸气,水蒸气遇冷液化,形成小水珠,将干冷的烧杯和蘸有澄清石灰水的烧杯倒置于火焰上方。观察到干冷的烧杯内壁出现水雾和澄清石灰水变浑浊,由此确定甜叶菊苷中一定含有碳、氢元素;
(1)装置中C中的氧化铜能确保甜叶菊苷中的碳元素完全转化为二氧化碳,空气中的二氧化碳也能被氢氧化钠吸收,所以实验前要通一会儿氮气,目的是:排除装置中的空气;
(2)过氧化氢在二氧化锰的催化作用下分解生成水和氧气,化学方程式为:2H2O2 ![]() 2H2O+O2
2H2O+O2![]() ;
;
(3)D装置中增加的质量是水的质量,E装置中增加的质量是二氧化碳的质量,所以二氧化碳中碳元素的质量=![]() ,水中的氢元素的质量=
,水中的氢元素的质量=![]() ,根据质量守恒定律可知,甜叶菊苷中碳元素的质量=2.2g,氢元素的质量=0.3g,2.2g+0.3g<4.02g,甜叶菊苷中还存在氧元素,氧元素的质量=4.02g﹣0.3g﹣2.28g=1.44g;
,根据质量守恒定律可知,甜叶菊苷中碳元素的质量=2.2g,氢元素的质量=0.3g,2.2g+0.3g<4.02g,甜叶菊苷中还存在氧元素,氧元素的质量=4.02g﹣0.3g﹣2.28g=1.44g;
(4)没有F装置,空气中的二氧化碳会进入E装置中,碳元素的质量偏大,氧元素质量测定结果的影响是偏小。

【题目】某化学兴趣小组为测定一批石灰石样品中碳酸钙的质量分数,取10g石灰石样品,把40g稀盐酸分4次加入样品中(样品中的其它成分既不与盐酸反应,也不溶于水),充分反应后经过滤、干燥、称量等操作,实验数据如下表:
实验 | 第一次 | 第二次 | 第三次 | 第四次 |
稀盐酸的用量 | 10g | 10 g | 10 g | 10 g |
剩余固体的质量 | X g | 4 g | 2 g | 2 g |
(1)表中X的值 为________g;
(2)该石灰石样品中碳酸钙的质量分数为_______;
(3)计算实验过程中产生二氧化碳气体的质量_______。(写出计算过程)