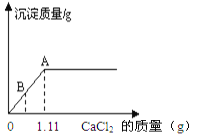
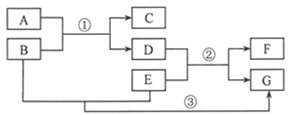
题目内容
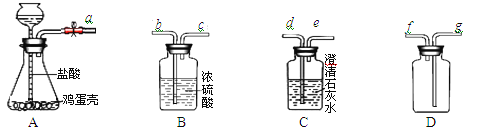
【题目】(4分)化学小组探究镁、铁、铜三种金属的活动性顺序,设计了下图所示实验方案。
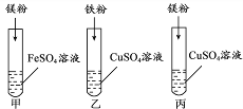
(1)试管乙中观察到的现象是 ,反应的化学方程式为 。
(2)同学们经讨论后认为该方案可以优化, 试管的实验是多余的。
(3)去掉多余的实验,同学们将另两只试管中反应后的物质倒入同一大烧杯中,一段时间后过滤,向滤渣中加入稀硫酸,有气泡产生,则滤渣的成分可能是 。
【答案】(1)溶液有蓝色变为浅绿色,生成红色固体 Fe+CuSO4=FeSO4+Cu
(2)丙 (3)Cu、Fe;Cu、Fe、Mg
【解析】
试题分析:(1)铁与硫酸铜溶液反应,生成铜和硫酸亚铁,现象为铁粉表面覆盖红色物质,溶液由蓝色变为浅绿色;(2)丙试管的实验是多余的,甲和乙已经得出三种金属活动性顺序;(3)向滤渣中加入稀硫酸,有气泡产生,说明滤渣中含有铁或铁和镁,而铁、镁都优先将硫酸铜中的铜置换出来,若镁将铜置换完后,还有剩余,镁会置换出硫酸亚铁中的铁。所以滤渣的成分可能是Cu、Fe或Cu、Fe、Mg

 发散思维新课堂系列答案
发散思维新课堂系列答案【题目】(8分)人类的日常生活和工农业生产离不开水。
(1)取2个烧杯,各盛大半烧杯浑浊的天然水,向其中1个烧杯中加入3药匙明矾粉末,搅拌溶解后,静置一段时间,观察到的现象是 。
(2)如图所示,在电解器玻璃管内加满水,接通直流电源,一段时间后切断电源,用燃着的木条分别在两个玻璃管尖嘴口检验电解反应中产生的气体。完成下表:
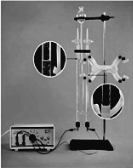
气体体积 | 用燃着的木条检验气体时的现象 | |
正极端玻璃管 | mL | |
负极端玻璃管 | 10mL |
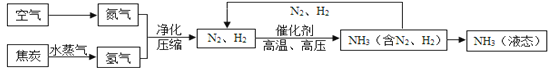
(3)工业上可以利用甲烷与水蒸气在一定条件下发生反应来制取氢气,化学方程式为CH4+H2O一定条件CO+3H2。若用该方法制取150kg氢气,消耗甲烷的质量是多少?(写出计算过程)
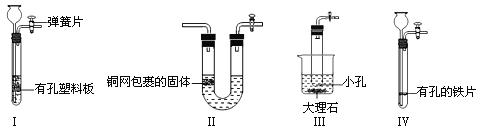
【题目】(8分)常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体。小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物。
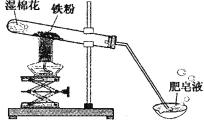
(1)试管尾部放一团湿棉花的目的是_______________。
(2)探究生成的气体是什么?
用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中。说明生成的气体是______________。
(3)探究试管中剩余固体成分是什么?
【查阅资料】
常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
能否被磁铁吸引 | 否 | 否 | 能 |
【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引。
【猜想与假设】猜想一:剩余固体是Fe与Fe3O4;猜想二:剩余固体是_____________
【实验探究】
实验操作 | 实验现象及结论 |
【实验结论】铁和水蒸气反应的化学方程式为_________________________________。
【反思与交流】该黑色固体不可能是Fe2O3,理由是___________________________。