题目内容
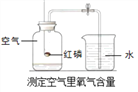
【题目】实验室里,在一个具有刻度和可以滑动的活塞的玻璃管中放入白磷(过量,白磷燃烧所需的最低温度为40 ℃,燃烧现象及产物均与红磷相同 ),将玻璃管固定好,放在盛有80 ℃热水的烧杯上,实验装置如图1所示,试回答下列问题。
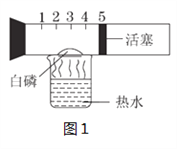

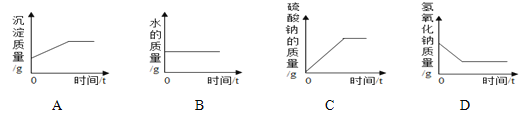
(1)整个实验过程中,可以观察到的现象有:
①玻璃管内______________________;
②活塞________________________________________________;
③活塞最后约停在刻度_______处。
白磷在反应过程中要过量的原因是_________________________________。
(2)图2为书本上测定空气中氧气含量的实验装置,图1和图2相比,你认为哪种装置更好?理由是什么?___________________________。
【答案】 产生大量白烟 先向右移动,再向左移动 4 耗尽玻璃管中的氧气 图1 活塞更易移动,实验误差更小
【解析】(1)实验过程中,可以观察到的现象有:①玻璃管内白磷燃烧,产生大量的白烟;②由于白磷燃烧放出了大量的热,活塞向右移动,又由于白磷燃烧消耗了氧气,冷却后压强减小,活塞再向左移动;③由于空气中氧气约占空气的![]() ,活塞最后约停在刻度4处;白磷在反应过程中要过量的原因是:耗尽玻璃管中的氧气;(2)图1和图2相比,图1装置更好,原因由是:活塞更易移动,实验误差更小。
,活塞最后约停在刻度4处;白磷在反应过程中要过量的原因是:耗尽玻璃管中的氧气;(2)图1和图2相比,图1装置更好,原因由是:活塞更易移动,实验误差更小。

 阅读快车系列答案
阅读快车系列答案【题目】化学课后,化学兴趣小组的同学在整理实验桌时,发现有一瓶氢氧化钠溶液没有塞橡皮塞,征得老师同意后,开展了以下探究:
[提出问题1] 该氢氧化钠溶液是否变质了呢?
[实验探究1]
实验操作 | 实验现象 | 实验结论 |
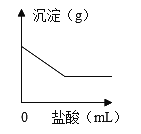
取少量该溶液于试管中,向溶液中滴加稀盐酸,并不断振荡。 | _____________ | 氢氧化钠溶液一定变质了。 |
[提出问题2] 该氢氧化钠溶液是全部变质还是部分变质呢?
[猜想与假设]
猜想1:氢氧化钠溶液部分变质。 猜想2:氢氧化钠溶液全部变质。
[查阅资料] ⑴ 氯化钙溶液呈中性。
⑵ 氯化钙溶液能与碳酸钠溶液反应(方程式):________________________。
[实验探究2]
实验步骤 | 实验现象 | 实验结论 |
⑴取少量该溶液于试管中,向溶液中滴加过量的氯化钙溶液,并不断振荡。 | 有________生成 | 说明原溶液中一定有碳酸钠。 |
⑵取步骤⑴试管中的少量上层清液,滴加酚酞溶液。 | _____________ | 说明原溶液中一定有______。 |
[实验结论] 该氢氧化钠溶液_______(填“部分”或“全部”)变质。
[反思与评价] ⑴氢氧化钠溶液露置于空气中容易变质,请写出相关反应的化学方程式:_________。
⑵在上述[实验探究2]中,小明提出可用氢氧化钙溶液代替氯化钙溶液,你认为该方案________(填“可行”或“不可行”)。
[理解与应用] 氢氧化钠溶液容易变质,必须密封保存。