题目内容
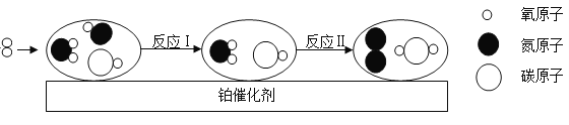
【题目】某日报有题为“学校化学实验室也是污染源”的报道,文章指出:全国数以万计的高校、中学的化学实验室每天都排放着成分复杂的污染物。为此某校化学研究小组拟进行如下试验,以粗略测试刚做完实验的实验室(甲)空气中全部酸性气体的含量。
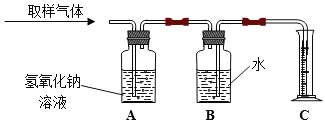
步骤:
(1)取样:因试验在另一间没有污染的实验室(乙)中进行,请你设计取出适量化学实验室(甲)空气样品的方法:_________________________________________。
(2)按图装置取得的气体进行实验,问:图中装置A的作用是______________________;
装置C的作用是______________________________________。
若酸性气体中含有二氧化硫,请写出其在A装置中反应的化学方程式:______________________。
(3)计算:若取样气体为100毫升,装置C读数为99.0毫升,则实验室(甲)空气中总酸性气体体积含量约为_________%。
分析:①一般空气中含二氧化碳约为0.03%,此样品中由实验室废气产生的酸性气体约为______%。
②请提出你在进行化学实验时,减少实验室对人类生存环境污染的一种做法:__________。
【答案】 使用注射器;或使用装满水的瓶子,进入实验室后倒去水,用干布擦拭;或使用气囊等 吸收样品中的酸性气体 测量吸收酸性气体后剩下气体的粗略体积 2NaOH+SO2→Na2SO3+H2O 1% 0.97% 控制实验室药品用量;不乱倒废液、乱扔废物等
【解析】氢氧化钠溶液容易与酸性气体反应,所以主要是吸收酸性气体的,根据气体排出水的体积可测出气体体积,从而算出剩余气体的体积;根据剩余气体排出水的体积算出酸性气体的体积,(1)取出适量化学实验室(甲)空气样品的方法:使用注射器;或使用装满水的瓶子,进入实验室后倒去水,用干布擦拭;或使用气囊等 (2)氢氧化钠溶液显碱性,是吸收二氧化碳气体的,装置C的作用是:通过排出水的体积可算出剩余气体的体积;A装置中反应的化学方程式2NaOH+SO2═Na2SO3+H2O;(3)根据气体100mL,装置C的读数为99.0mL可知酸性气体为1mL;①根据一般空气中含二氧化碳约为0.03%,此样品中由实验室废气产生的酸性气体约为0.97%.②减少实验室对人类生存环境污染的一种做法是:尾气处理后再排放,减少药品使用,既减少了尾气排放也节约了药品.

【题目】某化学兴趣小组围绕“酸碱中和反应”,在老师引导下开展探究活动.
探究:证明氢氧化钠溶液与稀盐酸确实能发生反应.
【方案1】测定稀盐酸与NaOH溶液混合前后的pH.
测定某NaOH溶液的pH,pH大于7.将一定量的稀盐酸加入该NaOH溶液中,混合均匀后测定其pH,发现pH减小了,但仍然大于7,小组中有的同学认为根据这个测定结果不可以认为稀盐酸与NaOH溶液发生了反应,你认为他的理由____.经过讨论后,他们向溶液中又加入一定量的稀盐酸,混合均匀后测定其pH,pH小于7.
结论:稀盐酸与氢氧化钠溶液发生了化学反应,并且稀盐酸过量.
【方案2】借助于无色酚酞试液.
【药品仪器】
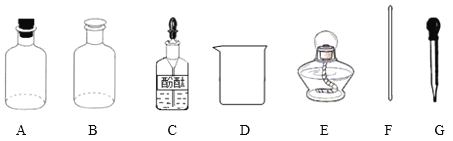
①取____(选填“A”或“B”)中试剂加入至D中,滴加2滴酚酞试液,溶液呈红色;
②用胶头滴管向①中溶液滴加稀盐酸,红色消失;
③用F蘸取②中溶液,在酒精灯上灼烧,有白色固体产生.
【思考拓展】
(1)如不使用酸碱指示剂,进一步确认步骤③中的白色固体不是氢氧化钠的方法是:____;
(2)探究步骤②中无色溶液中稀盐酸是否过量.
根据上述反应过程中溶液变成无色,不能确定稀盐酸是否过量,兴趣小组同学又分别选取了AgNO3溶液、紫色石蕊试液、铁锈粉末设计实验方案,请你分析并判断:
实验方案 | 实验步骤 | 现象 | 结论 |
① | 取样,加入适量的AgNO3溶液 | 出现白色沉淀 | 稀盐酸过量 |
② | 取样,加入几滴紫色石蕊试液 | 溶液变红 | 稀盐酸过量 |
③ | 取样,加入铁锈粉末 | 稀盐酸过量 |
方案③中反应的化学方程式____.上述设计方案中,不正确的是____(填“①”、“②”或“③”),错误的原因是____;
(3)碱与酸反应不一定都无明显现象,写出一个有沉淀生成的中和反应:____.
【题目】小东从海边捡来一些嵌有砂砾的贝壳(主要成分是CaCO3),为测定碳酸钙的含量,他做了如下实验:首先称取50g贝壳样品,然后将150mL的盐酸分5次加入(假设其余杂质均不与盐酸反应),实验过程中的数据记录如下:
稀盐酸的体积 | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 |
剩余固体质量 | 40.0g | X | 20.0g | 10.0g | 5.0g |
(1)X= g;
(2)小东测得贝壳样品中碳酸钙的质量分数是 ;
(3)若把二氧化碳收集起来,共有 g.