题目内容
【题目】水是生命之源!“珍惜水、节约水、爱护水”是每个公民应尽的义务和责任。
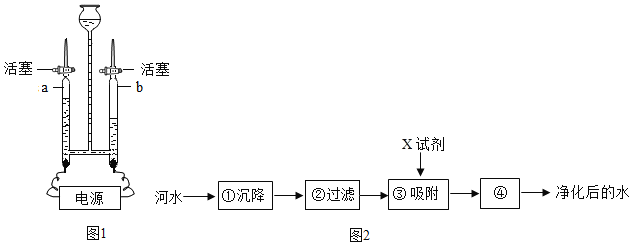
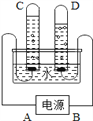
(1)用如图1所示装置进行电解水的实验,a、b两玻璃管中收集到的气体质量比为___反应的化方程式为__,该实验证明水是由__组成的;
(2)饮用硬度过大的水不利于人体键康,在生活中可用_____区分硬水和软水;
(3)如图2是自来水厂净化水的主要步骤。有关说法错误的是_____(填字母);
A步骤①中可加入明矾作絮凝剂 B X试剂可以是活性炭
C步骤④的作用是消毒杀菌 D净化后的水为纯净物
(4)请列举一例生活中节约用水的具体做法_____。
【答案】8:1 2H2O![]() 2H2↑+O2↑ 氢元素和氧元素 肥皂水 D 用洗菜水浇花
2H2↑+O2↑ 氢元素和氧元素 肥皂水 D 用洗菜水浇花
【解析】
(1)电解水产生的氧气和氢气的体积比是1:2,从图中a管产生的气体少,b管产生的气体多,得出a、b两玻璃管中收集到的气体体积比为1:2,质量比为8:1;水在通电的条件下生成氢气和氧气,反应的化学方程式为2H2O![]() 2H2↑+O2↑;水电解时,生成氢气和氧气,氢气是由氢元素组成,氧气是由氧气元素组成,在化学反应中,元素的种类不变,该实验证明水是由氢元素和氧元素组成的;
2H2↑+O2↑;水电解时,生成氢气和氧气,氢气是由氢元素组成,氧气是由氧气元素组成,在化学反应中,元素的种类不变,该实验证明水是由氢元素和氧元素组成的;
(2)水样加入肥皂水搅拌,泡沫多的是软水,泡沫少的硬水,生活中用肥皂水区分硬水和软水;
(3)A 步骤①中可加入明矾作絮凝剂,用于悬浮性杂质的沉降,故A正确;
B X试剂可以是活性炭,具有吸附性,除去水中的色素和异味;故B正确;
C 步骤④的作用是消毒杀菌,故C正确;
D 净化后的水为混合物,因为水中还有可溶性杂质,故D错误。故选D;
(4)生活中可以采用“一水多用”来节约用水,具体做法有用洗菜水浇花等;

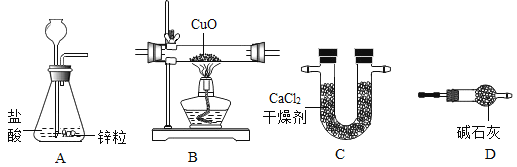
【题目】利用干燥而纯净的氢气还原氧化铜的实验测定水的质量组成。其装置如下图所示:完全反应后其实验测定的数据如下表所列(必要时装置可重复使用)。
实验前 | 实验后 | |
(氧化铜+玻璃管)的质量/g | 75.6 | 69.2 |
(氯化钙+U型管)的质量/g | 100.8 | 118.0 |
试回答:
(1)A中反应容器的仪器名称是:__________。
(2)装置正确的连接顺序(自左向右)是(填字母)A-________--________--________--________。
(3)连接好装置并检查气密性装好药品后在加热前的必要操作是:________。
(4)生成水中氢元素的质量为________________________。
(5)如果没有实验装置D,实验测得水中氢的质量________(填“偏大”“偏小”或者“不变”)。
(6)本实验装置从安全角度考虑存在的缺陷是:________________________。