题目内容
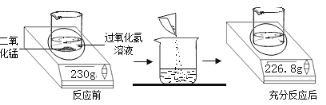
【题目】为测定实验室中某过氧化氢溶液的溶质质量分数,取100.0g过氧化氢溶液放入小烧杯中,然后进行如图所示的实验.请计算:
①反应后产生气体的物质的量 ⑴ 。
②该过氧化氢溶液的溶质质量分数 ⑵ 。(请根据化学方程式列式计算)
【答案】⑴0.1mol; (2)6.8%
【解析】
试题分析:(1)因为反应后物质减少的质量就是生成的气体的质量:故230g-226.8g=3.2g;①反应后产生气体的物质的量为3.2g/32g/mol=0.1mol
⑵设:含H2O2的物质的量为Xmol.
2H2O2 ![]() 2H2O+O2↑
2H2O+O2↑
2 1
Xmol 0.1 mol
2/ X =1/ 0.1
X=0.2(mol)
过氧化氢的质量为0.2mol×34g/mol=6.8g
过氧化氢溶液溶质的质量分数为:6.8g÷100.0g×100%=6.8%

练习册系列答案
相关题目