题目内容
【题目】I.如图是一瓶医用注射盐水标签的部分内容。完成下列填空:
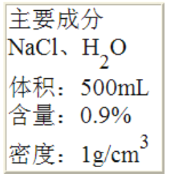
(1)氯化钠中钠、氯元素的质量比是_____;
(2)氯化钠中钠元素的质量分数是_____(精确到0.1%);
(3)该瓶盐水能给病人提供氯化钠的质量是_____g;
(4)该瓶盐水能给病人提供钠元素的质量是_____g (精确到0.1g)。
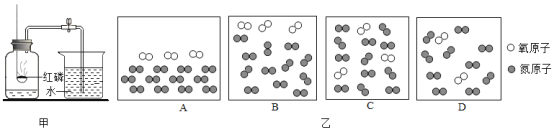
Ⅱ.在一定条件下,向一密闭容器内加入ABCD四种物质各20克,充分反应后测定其质量,得到数据如下,回答下列有关问题:
物质 | A | B | C | D |
反应前质量(克) | 20 | 20 | 20 | 20 |
反应后质量(克) | 20 | 30 | 未知 | 14 |
(1)这一反应类型是_____,未知值为_____。
(2)由表中数据分析可知,A可能没有参加化学反应,也可能是该反应的_____。
(3)写出一例与上述反应类型相同的反应化学方程式_____。
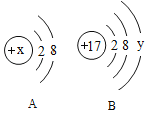
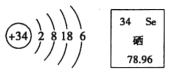
Ⅲ.如图A、B、C三种物质都含有同一种元素,B是单质, A、C都是氧化物,C是一种黑色固体物质。请回答:
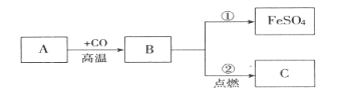
(1)写出A的化学式_____;
(2)写出反应②的化学方程式为_____;
(3)指明反应①基本反应类型_____。
【答案】![]() 39.3% 4.5 1.8 化合反应 16 催化剂
39.3% 4.5 1.8 化合反应 16 催化剂 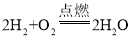 Fe2O3(或Fe3O4)
Fe2O3(或Fe3O4) 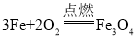 置换反应
置换反应
【解析】
反应后A的质量不变,可能是催化剂,也可能既不是催化剂,也不是反应物和生成物;反应后B质量增加10g,是生成物;反应后D质量减小6g,是反应物;根据质量守恒定律可知,C是反应物,参加反应的质量为![]() ,未知=16g;单质B经过反应①会转化成硫酸亚铁,B点燃后会生成黑色固体C,且C是氧化物,B是铁,C是四氧化三铁,氧化物A和一氧化碳高温会生成铁,A、B、C三种物质都含有同一种元素,A是氧化铁(或四氧化三铁)。
,未知=16g;单质B经过反应①会转化成硫酸亚铁,B点燃后会生成黑色固体C,且C是氧化物,B是铁,C是四氧化三铁,氧化物A和一氧化碳高温会生成铁,A、B、C三种物质都含有同一种元素,A是氧化铁(或四氧化三铁)。
I.(1)氯化钠中钠、氯元素的质量比是![]()
(2)氯化钠中钠元素的质量分数是![]()
(3)该瓶盐水能给病人提供氯化钠的质量是![]()
(4)该瓶盐水能给病人提供钠元素的质量是![]()
Ⅱ.(1)反应后A的质量不变,可能是催化剂,也可能既不是催化剂,也不是反应物和生成物;反应后B质量增加10g,是生成物;反应后D质量减小6g,是反应物;根据质量守恒定律可知,C是反应物,参加反应的质量![]() ,未知=16g,故这一反应类型是化合反应,未知值为16。
,未知=16g,故这一反应类型是化合反应,未知值为16。
(2)由表中数据分析可知,反应后A的质量不变,A可能没有参加化学反应,也可能是该反应的催化剂。
(3)氢气在氧气中点燃生成水,反应类型也是化合反应,反应化学方程式为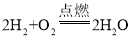 。
。
Ⅲ.A、B、C三种物质都含有同一种元素,单质B经过反应①会转化成硫酸亚铁,B点燃后会生成黑色固体C,且C是氧化物,B是铁,C是四氧化三铁,氧化物A和一氧化碳高温会生成铁,A、B、C三种物质都含有同一种元素,A是氧化铁(或四氧化三铁)。
(1)氧化物A和一氧化碳高温会生成铁,A、B、C三种物质都含有同一种元素,A是氧化铁(或四氧化三铁),故A的化学式Fe2O3(或Fe3O4)。
(2)反应②是铁和氧气在点燃的条件下生成四氧化三铁,反应的化学方程式为
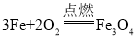 。
。
(3)反应①可以是硫酸和铁反应生成硫酸亚铁和氢气,反应是单质和化合物反应生成另一种单质和另一种化合物的反应,故基本反应类型为置换反应。

【题目】钢铁工业是国家工业的基础.
(1)图1是教材中炼铁高炉及炉内化学变化过程示意图,根据图示回答问题.若图1中采用的铁矿石的主要成分为氧化铁,请写出A区和B区所发生主要反应的化学方程式:A区_____;B区(焦炭的作用)_____、_____.
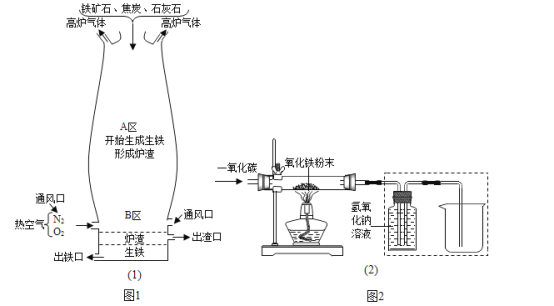
(2)某兴趣小组在实验室中模拟炼铁化学原理的实验,对固体产物成分等进行探究.
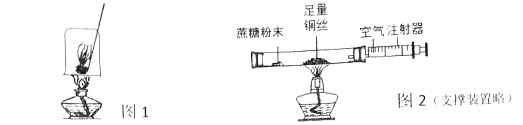
[设计实验]用一氧化碳还原纯净的氧化铁 粉末,实验装置如图2.
[进行实验]该小组按上述实验设计,在一定温度下进行了实验,测得下列数据:①反应前玻璃管和内盛氧化铁粉末的总质量66.0g(玻璃管的质量为60.0g) ②反应后玻璃管和内盛黑色固体的总质量65.8g(冷却到室温称量).
[分析与讨论]本实验中,玻璃管内固体粉末由红色全部变为黑色.小明同学认为该黑色固体全部是铁,但小华同学提出了质疑,于是大家提出查阅资料.
[查阅资料]
物质 性质 | 四氧化三铁 | 氧化亚铁 | 氧化铁 | 铁粉 |
颜色 | 黑色 | 黑色 | 红色 | 黑色 |
能否被磁铁吸引 | 能 | 不能 | 不能 | 能 |
①一氧化碳还原氧化铁的固体产物的成分与反应温度、反应时间等因素有关.
②一氧化碳还原氧化铁的实验过程中固体产物可能有四氧化三铁、氧化亚铁、铁.
③四氧化三铁、铁粉都能被磁铁吸引,而氧化亚铁、氧化铁均不能被磁铁吸引.
[实验与猜想]
①该小组同学将反应后的黑色固体研磨后,再用磁铁吸引,发现黑色固体粉末全部能被吸引,则该黑色固体粉末中不可能含有_____和_____.
②进行猜想:黑色固体粉末可能
a.全部为铁 b._____ c._____.
[得出结论]
通过实验中获得的数据进行计算,得出黑色固体粉末为(写名称)_____.
计算过程:
[反思与评价]
①一氧化碳还原氧化铁的实验中,若要得到铁可适当提高反应温度和延长反应时间.
②实验装置图中采用虚线框内的装置,其作用有_____.
A 收集一氧化碳 B 吸收二氧化碳 C 检验二氧化碳.