题目内容
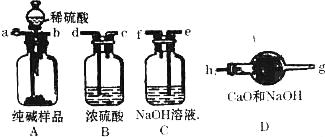
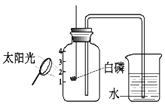
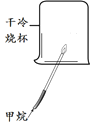
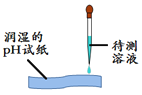
【题目】在四只试管中分别装有滴有酚酞的饱和石灰水,进行下列实验。
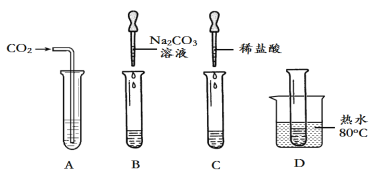
依据实验回答问题:
(1)实验中能观察到相同现象的是______(填序号)。
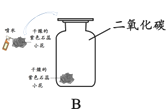
(2)B中发生反应的化学方程式为______。
(3)证明盐酸与氢氧化钙发生反应的现象是______。
【答案】BD Ca(OH)2+Na2CO3=CaCO3↓+2NaOH C中溶液由红色逐渐变为无色
【解析】
氢氧化钙溶液显碱性,能使无色酚酞变红;实验A中二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,当二氧化碳过量时会和碳酸钙和水反应生成可溶性的碳酸氢钙,实验中先观察到出现白色沉淀,红色逐渐消失,一段时间后白色沉淀消失,溶液又变为红色;实验B中碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,观察到有白色沉淀生成,溶液红色不消失;实验C中稀盐酸和氢氧化钙反应生成中性的氯化钙和水,稀盐酸少量时无现象,稀盐酸足量或过量时观察到红色逐渐变为无色;实验D中,由于氢氧化钙的溶解度随温度的升高而减小,将强氧化钙饱和溶液置于80℃的热水中,会有白色晶体析出。
(1)由上分析可知,能观察到相同现象的是BD;
(2)B中发生的是氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式为Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(3)由分析可知,证明盐酸与氢氧化钙发生反应的现象是C中溶液由红色逐渐变为无色。

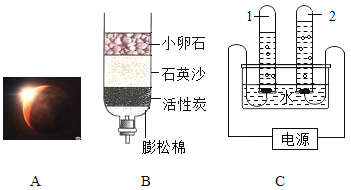
【题目】在高温下,铁与水蒸气能发生反应生成一种常见的铁的氧化物和一种气体.某兴趣小组请你参与研究:铁与水蒸气反应一段时间后剩余固体物质的成分、性质及再利用.
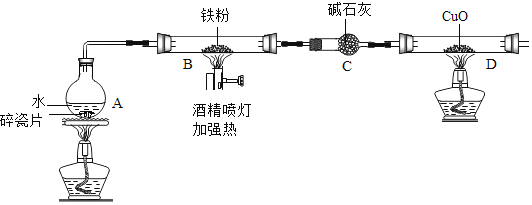
(1)(推断)观察到D中黑色固体变红,则B中生成的气体是______.
(2)探究B装置中剩余固体成分是什么?
(查阅资料)
(1)碎瓦片能防爆沸,碱石灰是氧化钙和氢氧化钠的混合物
(2)铁的氧化物中,只有Fe2O3是红棕色,其余均为黑色,只有Fe3O4能被磁铁吸引.
(3)Fe3O4+8HCl=FeCl2+2FeCl3+4H2O、Fe3O4+4H2SO4=FeSO4+Fe2(SO4)3+4H2O
(初步探究)B装置中剩余固体为黑色,能全部被磁铁吸引
(猜想与假设)
猜想一:剩余固体是Fe3O4
猜想二:剩余固体是______
(实验探究)
实验操作 | 实验现象及结论 |
______ | ______ |
(实验结论)铁与水蒸气反应的化学方程式为______.