题目内容
【题目】现有Ca(OH)2、CaCO3和一些杂质(不与稀盐酸反应)组成的混合物共15g,取某浓度的稀盐酸,逐滴滴加到混合物中,充分反应,测得稀盐酸的质量与反应生成气体的质量,关系如图所示:
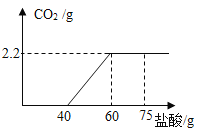
(1)生成CO2的质量是_______g;
(2)计算混合物中CaCO3的质量分数 (写出计算过程,结果精确到0.1%)_____;
(3)所取稀盐酸的浓度是______,欲配制100g该浓度的稀盐酸,需要溶质质量分数为36.5%的盐酸_______g。
【答案】(1)2.2;(2)33.3%;(3)18.25%;50
【解析】
(1)由图可知,生成二氧化碳的质量为2.2g,故填2.2。
(2)解:设参加反应的CaCO3的质量为x。
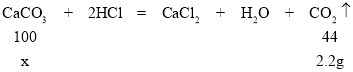
![]()
x=5g
混合物中CaCO3的质量分数为:![]() ×100%≈33.3%
×100%≈33.3%
答:混合物中CaCO3的质量分数为33.3%。
(3)解:设参加反应的纯净HCl的质量为y

![]()
y=3.65g
由图可知,生成2.2g二氧化碳时,与碳酸钙反应的盐酸的质量为60g40g=20g
所取稀盐酸的浓度为![]() ×100%=18.25%
×100%=18.25%
配制100g该浓度的稀盐酸,需要溶质质量分数为36.5%的盐酸质量为100g×18.25%÷36.5%=50g
答:所取稀盐酸的浓度为18.25%,需要溶质质量分数为36.5%的盐酸质量为50g。

【题目】元素周期表和化学用语都是学习化学的重要工具。回答下列问题:
3 Li 锂 | 4 Be 铍 | 5 B 硼 | 6 C 碳 | 7 N 氮 | 8 O 氧 | 9 F 氟 | 10 Ne 氖 |
11 Na 钠 | 12 Mg 镁 | 13 Al 铝 | 14 Si 硅 | 15 P 磷 | 16 S 硫 | 17 Cl 氯 | 18 Ar 氩 |
(1)同一周期中,从左到右各元素的原子最外层电子数逐渐__________。
(2)11—18号元素中稀有气体元素的符号是_______,此表中和它化学性质相似的是_________(填符号)。写出Mg2+ 数字“2”的含义:_______________。
(3)硫原子的结构示意图为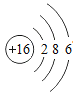 ,它在反应中易_____(填“得到”或“失去”)电子。它和钠元素形成的化合物的化学式为_______。
,它在反应中易_____(填“得到”或“失去”)电子。它和钠元素形成的化合物的化学式为_______。