题目内容
【题目】某校化学兴趣小组利用数字化传感器探究稀盐酸和氢氧化钠溶液的反应过程,测得烧杯中溶液的pH随滴加液体体积变化的曲线如图所示。下列说法错误的是( )
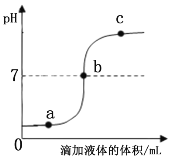
A. 图中a点所示溶液中,溶质是NaCl和HCl
B. 向图中c点所示溶液中滴加无色酚酞,溶液不变色
C. 该实验是将氢氧化钠溶液逐滴滴入到盛有稀盐酸的烧杯中
D. 由a点到b点的pH变化过程证明酸和碱发生了中和反应
【答案】B
【解析】
稀盐酸和氢氧化钠溶液反应生成氯化钠和水,如果稀盐酸过量,则溶液呈酸性,若氢氧化钠过量,则溶液呈碱性,若两者恰好完全反应,溶液呈中性。
A、a点时,pH小于7,溶液显酸性,则稀盐酸过量,部分稀盐酸和氢氧化钠反应生成氯化钠和水,则溶质是氯化钠和盐酸,故A正确;
B、c点溶液显碱性,滴加无色酚酞溶液时,溶液会变红色,故B不正确;
C、由pH变化情况可以看出,开始显酸性,b点时显中性,c点显碱性,故是将氢氧化钠加入到稀盐酸中,故C正确;
D、由a点到b点的pH变化逐渐变大,说明酸和碱发生了中和反应,酸过量,故D正确。故选B。

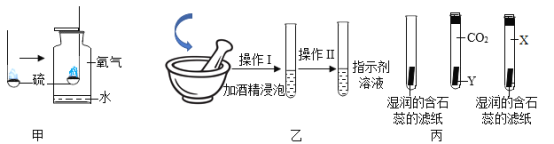
【题目】某化学兴趣小组的同学学习“灭火器原理”后,设计了如下图所示实验,并对反应后瓶中残留废液进行探究。
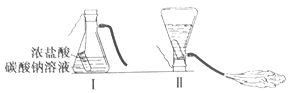
(提出问题)废液中所含溶质是什么?
(猜想与假设)
猜想1:废液中的溶质是NaCl、Na2CO3和HCl
猜想2:废液中的溶质只有NaCl
猜想3:废液中的溶质是NaCl、HCl
猜想4:废液中的溶质是______。
(讨论与交流)
小明认为猜想I无需验证就知道是错误的,他的理由是_____(请用化学方程式说明)。
(实验与结论)
(1)小亮同学为验证猜想3,取少量废液装入试管中,然后滴入酚酞溶液,发现溶液不变色,于是小亮认为猜想3正确。你认为他的结论____(填“正确”或“错误”),理由是______________。
请你另设计实验方案验证猜想3:
实验步骤 | 实验现象 | 实验结论 |
__________________ | __________________ | 猜想3正确 |
(2)验证猜想4,可选择的试剂有____________。
A.酚酞溶液B.氢氧化钾溶液C.稀硫酸D.氯化钡溶液
(拓展与应用)若废液中的溶质是NaCl和HCl,根据盐酸的性质,无需另加试剂,只要对废液进行____操作,即可从废液中得到NaCl固体。