题目内容
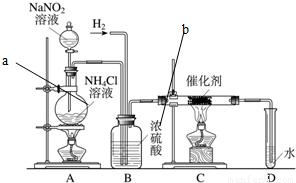
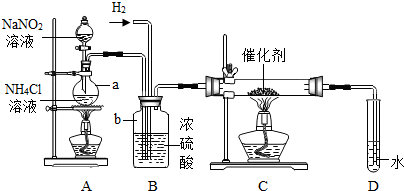 亚硝酸钠是实验室常用的试剂,实验室一般用亚硝酸钠溶液与氯化铵溶液反应来制取N2.N2的化学性质十分稳定,但在一定条件下能与H2部分化合生成NH3.下图为制取少量NH3的装置(制取H2的装置已略去):
亚硝酸钠是实验室常用的试剂,实验室一般用亚硝酸钠溶液与氯化铵溶液反应来制取N2.N2的化学性质十分稳定,但在一定条件下能与H2部分化合生成NH3.下图为制取少量NH3的装置(制取H2的装置已略去):(1)指出标号仪器的名称a
圆底烧瓶
圆底烧瓶
,b广口瓶
广口瓶
.(2)A装置中除有N2生成外,还有水等物质生成,写出反应的化学方程式
NaNO2+NH4Cl
N2↑+2H20+NaCl
| ||
NaNO2+NH4Cl
N2↑+2H20+NaCl
.
| ||
C装置的硬质试管中发生反应的化学方程式为
N2+3H2
2NH3
| ||
| △ |
N2+3H2
2NH3
.
| ||
| △ |
(3)写出实验室制取H2的化学方程式
Zn+H2SO4═ZnSO4+H2↑
Zn+H2SO4═ZnSO4+H2↑
,反应时N2和H2的最佳质量比是14:3
14:3
.(4)B中浓硫酸的作用是
干燥
干燥
.(5)用实验方法证明确实有NH3生成
向D中滴入无色酚酞溶液,酚酞变红
向D中滴入无色酚酞溶液,酚酞变红
.分析:(1)、识别仪器;
(2)、根据题干信息可知:反应物是NaNO2和NH4Cl,生成物是N2和H20,结合质量守恒定律可知:生成物还有NaCl,然后进行配平即可,注意反应条件.
(3)、这是教材氢气的实验制法,从教材可以找到.
(4)、浓硫酸的性质,从教材可知.
(5)、检验氨气的方法,从教材可知.
(2)、根据题干信息可知:反应物是NaNO2和NH4Cl,生成物是N2和H20,结合质量守恒定律可知:生成物还有NaCl,然后进行配平即可,注意反应条件.
(3)、这是教材氢气的实验制法,从教材可以找到.
(4)、浓硫酸的性质,从教材可知.
(5)、检验氨气的方法,从教材可知.
解答:解:
(1)、圆底烧瓶;广口瓶;
(2)根据质量守恒定律及题干信息可知,反应物是NaNO2和NH4Cl,生成物是N2和H20和NaCl,用观察法配平即可.故答案为NaNO2+NH4Cl
N2↑+2H20+NaCl;同样道理,N2+3H2
2NH3
(3)从教材可以找到氢气的实验制法,故答案为Zn+H2SO4═ZnSO4+H2↑,14:3;
(4)因为制取氮气时伴随有水蒸汽的生成,故硫酸的作用为干燥,
(5)这是氨气的检验方法,因为氨气的水溶液显碱性,所以加入酚酞变红.
(1)、圆底烧瓶;广口瓶;
(2)根据质量守恒定律及题干信息可知,反应物是NaNO2和NH4Cl,生成物是N2和H20和NaCl,用观察法配平即可.故答案为NaNO2+NH4Cl
| ||
| ||
| △ |
(3)从教材可以找到氢气的实验制法,故答案为Zn+H2SO4═ZnSO4+H2↑,14:3;
(4)因为制取氮气时伴随有水蒸汽的生成,故硫酸的作用为干燥,
(5)这是氨气的检验方法,因为氨气的水溶液显碱性,所以加入酚酞变红.
点评:这个题考查氢气的实验室制法、氨气的检验、浓硫酸的性质等内容,说明化学知识很零碎,要求学生平时加强记忆.

练习册系列答案
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案
相关题目
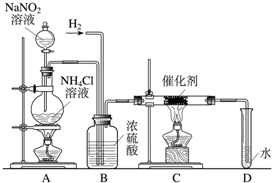
 亚硝酸钠是实验室常用的试剂,实验室一般用亚硝酸钠溶液与氯化铵溶液反应来制取N2.N2的化学性质十分稳定,但在一定条件下能与H2部分化合生成NH3.下图为制取少量NH3的装置(制取H2的装置已略去):
亚硝酸钠是实验室常用的试剂,实验室一般用亚硝酸钠溶液与氯化铵溶液反应来制取N2.N2的化学性质十分稳定,但在一定条件下能与H2部分化合生成NH3.下图为制取少量NH3的装置(制取H2的装置已略去):