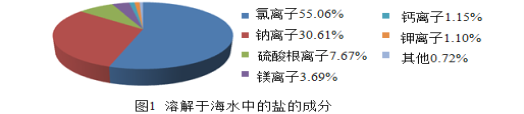
题目内容
【题目】三位同学分别用相同质量分数的稀盐酸,测定某石灰石样品中碳酸钙的质量分数(石灰石中的杂质既不与酸反应,也不溶于水)。
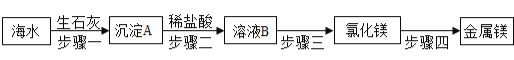
(1)小敏的方法可用如下流程表示,测得的碳酸钙的质量分数为 ;在过滤操作中,需要用到的玻璃仪器有 (选填序号)。
A.酒精灯、漏斗、玻璃棒B. 漏斗、玻璃棒、烧杯C. 酒精灯、试管、玻璃棒
![]()
(2)小华取10克样品,用如图甲实验装置进行实验,反应结束后,测得B装置质量增加了4.6克,根据上述数据,算得碳酸钙的质量分数,发现与事实严重不符,造成这种情况的可能原因是 _。

(3)小军用如图乙的实验装置进行实验,将20克稀盐酸加入到1.25克样品中,生成的CO2体积与反应时间的关系如图丙。已知本实验条件下CO2的密度为1.8克/升,求该石灰石样品中CaCO3的质量分数。
(4)求实验所用的稀盐酸溶质质量分数。
【答案】(1)79%(1分); B(2分);(2)B中吸收了二氧化碳带出的水蒸气或HCl气体 (1分)
(3)80%;(4)7.3%(2分)
【解析】
试题分析: (1)石灰石中的主要成分为碳酸钙,能与盐酸反应被溶解;由题意知:石灰石中杂质为2.1g,故碳酸钙质量为10g-2.1g=7.9g,其质量分数为![]() ×100%=79%;依据过滤操作的原理和装置可知:在过滤操作中,需要用到的玻璃仪器有B. 漏斗、玻璃棒、烧杯;(2)因为盐酸是溶液且具有挥发性,用盐酸制取的二氧化碳中含有水分和挥发出的氯化氢气体,碱石灰中的氢氧化钠和生石灰都能吸水且能与氢氧化钠反应,使B装置质量增加;(3)已知量生成的二氧化碳的质量,再用化学方程式即可求得未知量碳酸钙的质量;具体步骤如下:
×100%=79%;依据过滤操作的原理和装置可知:在过滤操作中,需要用到的玻璃仪器有B. 漏斗、玻璃棒、烧杯;(2)因为盐酸是溶液且具有挥发性,用盐酸制取的二氧化碳中含有水分和挥发出的氯化氢气体,碱石灰中的氢氧化钠和生石灰都能吸水且能与氢氧化钠反应,使B装置质量增加;(3)已知量生成的二氧化碳的质量,再用化学方程式即可求得未知量碳酸钙的质量;具体步骤如下:
生成CO2的m=ρV=1.8g/L×0.244L≈0.44g (1分)
设参加反应的碳酸钙质量为X,则
CaCO3+2HCl=CaCl2+CO2↑+H2O
100 44
X 0.44g
100:44=X:0.44g
X=1g
CaCO3%=1g/1.25g×100%=80%(1分)
(4)应找出盐酸完全反应时的盐酸质量及其氯化氢的质量,即可求得;已知量50g盐酸,对反应的碳酸钙质量为10g-5g=5g,再用化学方程式即可求得氯化氢的质量;
设参加反应的稀盐酸的质量分数为Y,则
CaCO3+2HCl=CaCl2+CO2↑+H2O
100 73
5g 50gY
100:73==5g:50gY
Y =7.3%(2分)

 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案