题目内容
【题目】(9分)镁及其化合物在生产、生活中应用广泛。
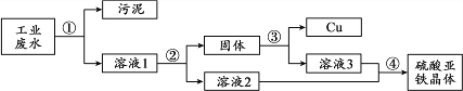
(1)从海水中提取金属镁,可按下图流程进行:

①下列说法正确的是 (填字母)。
A.步骤Ⅰ通过一步反应即可实现
B.步骤Ⅱ、Ⅲ、Ⅳ的目的是从海水中提纯氯化镁
C.步骤Ⅴ中化学能转化为电能
D.该流程涉及的基本反应类型有4种
②该流程中采取的一种降低成本且减少污染的措施是 。
(2)某化学兴趣小组对某种碱式碳酸镁晶体的组成进行探究。
【查阅资料】①碱式碳酸镁晶体可以表示为xMgCO3yMg(OH)2zH2O;②Mg(OH)2、MgCO3受热均能分解生成对应的氧化物;③碱石灰是固体氢氧化钠和生石灰等物质的混合物。
【设计实验】该小组同学设计了下图所示的实验装置,假设每步反应和吸收均进行完全。

【进行实验】取23.3g碱式碳酸镁晶体进行实验,步骤如下:
①连接好装置并检查气密性。
②装入药品,打开活塞K,通入一段时间空气。
③分别称量装置C、D的质量(数据见下表)。
装置C的质量 | 装置D的质量 | |
步骤③ | 292.4g | 198.2g |
步骤⑥ | 296.9g | 207.0g |
④关闭活塞K,点燃酒精灯,使碱式碳酸镁晶体完全分解。
⑤停止加热,同时打开活塞K,通入空气至恢复到室温。
⑥再次分别称量装置C、D的质量(数据见右表)。
【实验分析】
①装置A的作用为 ,装置D的作用为 。
②反应后,装置B中的剩余固体是 ,质量为 g。
③该碱式碳酸镁晶体[xMgCO3yMg(OH)2zH2O]中,x︰y︰z = (写最简整数比)。
【答案】(1)①B(错选、多选不给分)
②电解产生的Cl2用于生产HCl,与Mg(OH)2发生中和反应
(2)①除去空气中的二氧化碳和水 吸收反应生成的二氧化碳
②MgO(或氧化镁) 10
③4︰1︰4
【解析】
试题分析:(1)根据流程图分析判断。①A.步骤Ⅰ中碳酸钙不能通过一步反应生成氢氧化钙,错误; B.步骤Ⅱ、Ⅲ、Ⅳ的目的是从海水中提纯氯化镁,正确; C.步骤Ⅴ中是电能转化为化学能,错误; D.在此流程中,涉及的基本反应类型中没有置换反应,错误。故选B;②该流程中采取的一种降低成本且减少污染的措施是电解产生的Cl2用于生产HCl,与Mg(OH)2发生中和反应;
(2)【实验分析】①装置A的作用为除去空气中的二氧化碳和水,防止对反应物成分检验的干扰;装置D的作用为吸收反应生成的二氧化碳;②根据题中提供的信息知反应后,装置B中的剩余固体是氧化镁,质量为:23.3g-(296.9g-292.4g)-(207.0g-198.2g)=10g;③装置C增加的质量为生成水的质量,装置D增加的质量为生成二氧化碳的质量.
生成水的质量=296.9g-292.4g=4.5g,生成二氧化碳的质量=207.0g-198.2g=8.8g,
设碳酸镁的质量为x.生成氧化镁的质量为z
MgCO3═MgO+CO2↑
84 40 44
x z 8.8g
84/x=44/8.8g 40/z=44/8.8g
x=16.8g z=8g
则氢氧化镁产生氧化镁的质量=10g-8g=2.0g
设氢氧化镁的质量为y
Mg(OH)2═MgO+H2O
58 40
y 2.0g
58/y=40/2.0g
y=2.9g
所以xMgCO3yMg(OH)2zH2O中水的质量为=23.3g-16.8g-2.9g=3.6g
所以碳酸镁、氢氧化镁和水的质量比为:84x:58y:18z=16.8g:2.9g:3.6g 解得x:y:z=4:1:4.

【题目】(10分)常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体。小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物。
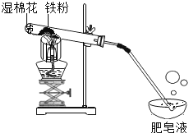
(1)试管尾部放一团湿棉花的目的是_______________。
(2)探究生成的气体是什么?
用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中。说明生成的气体是_________。
(3)探究试管中剩余固体成分是什么?
【查阅资料】
常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
能否被磁铁吸引 | 否 | 否 | 能 |
【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引。
【猜想与假设】猜想一:剩余固体是Fe与Fe3O4;猜想二:剩余固体是_____________。
【实验探究】
实验操作 | 实验现象及结论 |
【实验结论】铁和水蒸气反应的化学方程式为___________________________________。
【反思与交流】该黑色固体不可能是Fe2O3,理由是_______________________________。
【 拓展 】 把赤铁矿冶炼成铁,其主要反应原理是在高温下,一氧化碳夺取铁矿石里的氧,将铁还原出来,请写出化学反应方程式:______________________________________。