题目内容
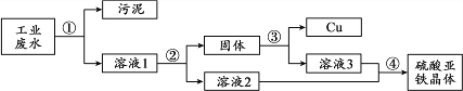
【题目】(3分)工业废水中含有硫酸亚铁、硫酸铜和污泥。某同学设计了利用废水制备硫酸亚铁晶体(FeSO4·7H2O)并回收铜的实验方案,流程如下:
已知:硫酸亚铁晶体受热易分解。
回答下列问题:
(1)步骤②中需加入的物质及目的是 。
(2)步骤③中发生反应的化学方程式为 。
(3)步骤④的操作是蒸发浓缩、降温结晶、 。
【答案】(1)过量的铁粉,把硫酸铜全部转化为铜 (2)Fe + H2SO4 = FeSO4 +H2↑ (3)过滤
【解析】
试题分析:(1)步骤②中加入过量的铁粉,目的是为了将硫酸铜中的铜完全转化为铜;(2)步骤③中发生反应的化学方程式为Fe + H2SO4 = FeSO4 +H2↑;(3)步骤④的操作是蒸发浓缩、降温结晶、过滤得到硫酸亚铁晶体。

【题目】(9分)镁及其化合物在生产、生活中应用广泛。
(1)从海水中提取金属镁,可按下图流程进行:

①下列说法正确的是 (填字母)。
A.步骤Ⅰ通过一步反应即可实现
B.步骤Ⅱ、Ⅲ、Ⅳ的目的是从海水中提纯氯化镁
C.步骤Ⅴ中化学能转化为电能
D.该流程涉及的基本反应类型有4种
②该流程中采取的一种降低成本且减少污染的措施是 。
(2)某化学兴趣小组对某种碱式碳酸镁晶体的组成进行探究。
【查阅资料】①碱式碳酸镁晶体可以表示为xMgCO3yMg(OH)2zH2O;②Mg(OH)2、MgCO3受热均能分解生成对应的氧化物;③碱石灰是固体氢氧化钠和生石灰等物质的混合物。
【设计实验】该小组同学设计了下图所示的实验装置,假设每步反应和吸收均进行完全。

【进行实验】取23.3g碱式碳酸镁晶体进行实验,步骤如下:
①连接好装置并检查气密性。
②装入药品,打开活塞K,通入一段时间空气。
③分别称量装置C、D的质量(数据见下表)。
装置C的质量 | 装置D的质量 | |
步骤③ | 292.4g | 198.2g |
步骤⑥ | 296.9g | 207.0g |
④关闭活塞K,点燃酒精灯,使碱式碳酸镁晶体完全分解。
⑤停止加热,同时打开活塞K,通入空气至恢复到室温。
⑥再次分别称量装置C、D的质量(数据见右表)。
【实验分析】
①装置A的作用为 ,装置D的作用为 。
②反应后,装置B中的剩余固体是 ,质量为 g。
③该碱式碳酸镁晶体[xMgCO3yMg(OH)2zH2O]中,x︰y︰z = (写最简整数比)。