题目内容
【题目】往100g硫酸和硫酸铜的混合液中,逐滴加入8%的氢氧化钠溶液直至过量,根据实验事实绘制了如图所示曲线,分析并计算:
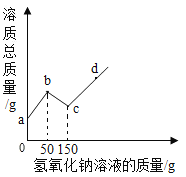
(1)a→b段表示氢氧化钠与混合物中的_____发生反应。
(2)求反应前混合液中硫酸铜的质量分数为__________。(写出计算过程)
【答案】 硫酸 16%
【解析】
硫酸和硫酸铜的混合液中加热氢氧化钠,氢氧化钠显和稀硫酸反应生成硫酸钠和水, 后与硫酸铜反应生成氢氧化铜沉淀和硫酸钠;
(1)由上分析可知,a→b段表示氢氧化钠与混合物中稀硫酸反应;
(2)根据图,可以看出与硫酸铜反应的氢氧化钠溶液的质量为150g﹣50g=100g。
设反应前混合液中硫酸铜的质量分数为x。
2NaOH+CuSO4=Na2SO4+Cu(OH)2↓
80 160
8%×100g 100g×x
![]() =
=![]()
x=16%
答:(1)a→b段表示氢氧化钠与混合物中的 硫酸发生反应。
(2)反应前混合液中硫酸铜的质量分数为16%。

 中考解读考点精练系列答案
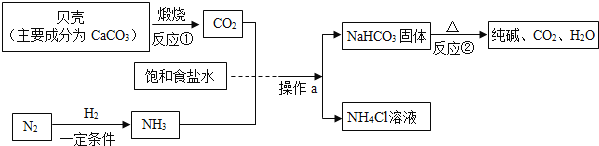
中考解读考点精练系列答案【题目】研究小组设计下列实验方案探究CO2与NaOH溶液是否发生反应。
方案一:
[查阅资料]
①乙醇不与NaOH、Na2CO3、CO2反应;
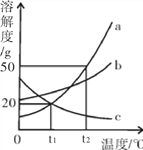
②25℃时,NaOH和Na2CO3在乙醇中的溶解度如下表:
物质 | NaOH | Na2CO3 |
溶解度/g | 17.3 | <0.01 |
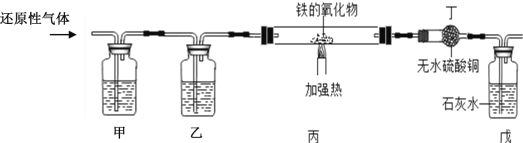
[实验装置] 如图1。
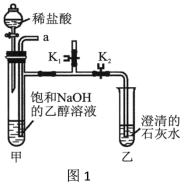
[实验步骤]
i.打开K1,关闭K2,从导管口a通入CO2气体,直至观察到饱和NaOH的乙醇溶液中产生大量沉淀,停止通CO2;
ii.从导管口a通入足量氮气;
iii.关闭K1,打开K2,向装置甲的试管中滴入足量的稀盐酸,观察装置乙的现象。
(1)步骤i产生沉淀的原因是___________________。
(2)步骤ii的目的是____________________。
(3)步骤iii装置乙中产生现象的原因是__________(用化学方程式表示)。
方案二:
[实验装置]
如图2(三颈瓶内集满CO2气体;装药品后的注射器B的活塞用夹子固定)。
[实验步骤]
按以下步骤完成实验,通过相对压强传感器测量瓶内压强的变化。整个实验过程的压强随时间变化如图3。
i.将注射器A内的NaOH溶液注入瓶中,测量压强直至不再改变;
ii.取下夹子,将注射器B内的盐酸注入瓶中,测量压强直至不再改变;
iii.将两个注射器的活塞都拉回原位,并都用夹子固定,测量压强直至不再改变。

(4)检查图2装置气密性的方法:____________。
(5)为缩短①→④中反应的时间,可采取的操作是______________。
(6)写出导致⑤→⑥压强变化的主要反应的化学方程式:________。
(7)步骤iii结束后瓶内压强比注入NaOH溶液前小,其原因是__________。
(8)请结合图3信息,说明NaOH与CO2发生了反应。_________。
【题目】酸中的H+没有被碱完全中和时生成的产物为酸式盐,可以继续和碱发生反应。同学们发现将一定量的NaOH溶液加入到NaHCO3溶液中,混合后无明显现象,如何证明两种物质发生了化学反应?反应后溶质有哪些?化学实验社的同学进行了下列探究:
(查阅资料)![]()
(实验探究1)用一定溶质质量分数的(NaHCO3,Na2CO3)溶液进行如下实验
|
| |
加稀盐酸 | A | 产生气泡 |
加无色酚酞溶液 | 溶液变红色 | 溶液变红色 |
加CaCl2溶液 | 无明显现象 | B |
上还表格中A处的实验现象为_____造成B处实验现象的原因是_____(用化学方程式表示)。
(猜想与假设)同学们对反应后溶液中溶质的成分进行了猜想
猜想1:![]()
猜想2:![]() 和
和![]()
猜想3:N![]() 和
和![]()
(实验探究2)
实验步骤 | 实验现象 | 实验结论 |
①取反应后溶液少许于试管中,请加过量的 | _____ | ①猜想2正确 ② |
②过滤后向滤液中加2﹣3滴无色酚酞试液 | _____ | |
③再滴加少量的_____ | _____ |
(表达与交流)对于没有明显现象的化学反应,可以通过检验有新物质生成或检验_____的方法来证明反应发生了。