题目内容
为了检测一种黄铜(铜锌合金)中含铜的质量分数,某化学兴趣小组同学称得黄铜样品10g,将它放入一定浓度足量的200g稀硫酸中,待反应完全后,称得剩余物质的质量为209.9g,问生氢气的质量是多少?并求出黄铜中铜的质量分数.(精确至0.1)(提示反应方程式为:Zn+H2SO4═ZnSO4+H2↑)
【答案】分析:首先根据质量守恒定律求出生成气体的质量即物质的总质量的减少的量,然后把生成的氢气的质量代入化学方程式进行计算就可求出有关的量.
解答:解:根据质量守恒定律生成氢气的质量为:200g+10g-209.9g═0.1g
设黄铜中锌的质量为ⅹ
Zn+H2SO4═ZnSO4+H2↑
65 2
x 0.1g
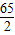 =
=
x= =3.25g
=3.25g
则铜的质量分数为 ×100%=62.5%
×100%=62.5%
答:生成的氢气的质量为0.1g,黄铜中铜的质量分数为62.5%.
点评:本题难度不是很大,主要考查了根据化学方程式的计算和质量守恒定律的应用,培养学生的分析能力和解决问题的能力.
解答:解:根据质量守恒定律生成氢气的质量为:200g+10g-209.9g═0.1g
设黄铜中锌的质量为ⅹ
Zn+H2SO4═ZnSO4+H2↑
65 2
x 0.1g
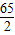 =
=
x=
 =3.25g
=3.25g则铜的质量分数为
 ×100%=62.5%
×100%=62.5%答:生成的氢气的质量为0.1g,黄铜中铜的质量分数为62.5%.
点评:本题难度不是很大,主要考查了根据化学方程式的计算和质量守恒定律的应用,培养学生的分析能力和解决问题的能力.

练习册系列答案
相关题目