题目内容
【题目】在两个盛有等质量的同种盐酸的烧杯中,分别加入NaOH和KOH各m克.已知加入NaOH的烧杯中NaOH和盐酸恰好完全反应.则加入KOH的那一烧杯中的溶液的pH值( )
A.小于7B.等于7C.大于7D.无法确定
【答案】A
【解析】
酸碱中和反应的实质是氢离子与氢氧根离子的反应,一定量的盐酸则氢离子一样多,由于氢氧化钠的相对分子质量(40)比氢氧化钾(56)小,相同质量时氢氧根的质量应该是氢氧化钠的多一些,氢氧化钠正好反应时氢氧化钾反应时应该量不足,也就是盐酸会有剩余,故溶液会呈酸性,pH会小于7。故选A。

练习册系列答案
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案
相关题目
【题目】均衡膳食,有利于人体健康.临近中考,小明为了给自己增加营养,制定了如下食谱:
主食 | 米饭 |
副食 | 红烧牛肉、花生米、清蒸鱼 |
饮料 | 牛奶 |
营养学家发现食谱中缺少富含维生素的食物,用你所学知识,建议小明应该增加的食物是( )
A.凉拌黄瓜B.红烧排骨C.烧豆腐D.炒鸡蛋
【题目】对比归纳是学习化学的重要方法。请你参与下列探究活动并回答问题:
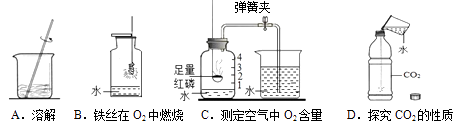
实验一:探究影响硫燃烧剧烈程度的因素。 |
| 硫在氧气中燃烧的化学方程式为; |
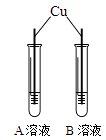
实验二:验证Fe>Cu>Ag金属活动性顺序 |
| 试管中A、B溶液的溶质为 |
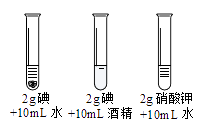
实验三:探究影响物质溶解性的因素。 |
| 振荡静置:B中固体易溶,A中几乎不溶。物质的溶解性与 |