题目内容
【题目】现有家用食用碱12g(主要成分Na2CO3,其它成分不与酸反应),向其中加入某未知浓度的稀盐酸100g,恰好完全反应,剩余物质的总质量为107.6g,反应过程如图所示,请计算:
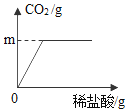
(1)该图中,m的值为______
(2)该食用碱中Na2CO3的质量_____
(3)该稀盐酸中溶质的质量分数_____.
【答案】4.4 10.6g 7.3%
【解析】
根据质量守恒定律,二氧化碳的质量为:100g+12g-107.6g=4.4g;
设该食用碱中Na2CO3的质量为x,稀盐酸中氯化氢的质量分数为y
Na2CO3+2HCl=2NaCl+CO2↑+H2O
106 73 44
X 100gy 4.4g
![]()
x=10.6g,y=7.3%
答:(1)该图中,m的值为 4.4;
(2)该食用碱中Na2CO3的质量为10.6g;
(3)该稀盐酸中溶质的质量分数为7.3%.

练习册系列答案
 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案
相关题目