题目内容
下列验证实验不能成功的是( )
A、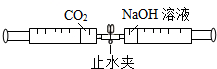 CO2能与烧碱溶液反应 | B、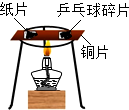 不同物质的着火点不同 | C、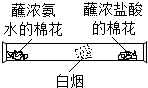 分子在不断运动 | D、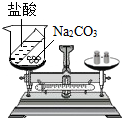 质量守恒定律 |
考点:化学实验方案设计与评价,碱的化学性质,分子的定义与分子的特性,质量守恒定律及其应用,燃烧与燃烧的条件
专题:简单实验方案的设计与评价
分析:A、根据二氧化碳和烧碱溶液反应生成碳酸钠和水,注射器内的压强变小进行解答;
B、根据纸片、乒乓球碎片的着火点不同,且铜片具有良好的导热性进行解答;
C、根据浓氨水、浓盐酸具有挥发性,分别挥发出氨气、氯化氢气体,二者会反应生成氯化铵固体进行解答;
D、根据盐酸和碳酸钠反应生成氯化钠、水和二氧化碳,有气体生成,所以验证质量守恒定律时要在密闭容器内进行解答.
B、根据纸片、乒乓球碎片的着火点不同,且铜片具有良好的导热性进行解答;
C、根据浓氨水、浓盐酸具有挥发性,分别挥发出氨气、氯化氢气体,二者会反应生成氯化铵固体进行解答;
D、根据盐酸和碳酸钠反应生成氯化钠、水和二氧化碳,有气体生成,所以验证质量守恒定律时要在密闭容器内进行解答.
解答:解:A、二氧化碳和烧碱溶液反应生成碳酸钠和水,注射器内的压强变小,所以在外界大气压的作用下,注射器的活塞会被向内推动,故A正确;
B、纸片、乒乓球碎片的着火点不同,且铜片具有良好的导热性,所以可用此实验验证不同物质的着火点不同,故B正确;
C、浓氨水、浓盐酸具有挥发性,分别挥发出氨气、氯化氢气体,二者会反应生成氯化铵固体,会看到有白烟生成,所以可以验证分子在不断运动,故C正确;
D、盐酸和碳酸钠反应生成氯化钠、水和二氧化碳,有气体生成,所以验证质量守恒定律时要在密闭容器内,而不是烧杯内,故D错误.
故选:D.
B、纸片、乒乓球碎片的着火点不同,且铜片具有良好的导热性,所以可用此实验验证不同物质的着火点不同,故B正确;
C、浓氨水、浓盐酸具有挥发性,分别挥发出氨气、氯化氢气体,二者会反应生成氯化铵固体,会看到有白烟生成,所以可以验证分子在不断运动,故C正确;
D、盐酸和碳酸钠反应生成氯化钠、水和二氧化碳,有气体生成,所以验证质量守恒定律时要在密闭容器内,而不是烧杯内,故D错误.
故选:D.
点评:解答本题要掌握各种物质的性质方面的内容,只有这样才能对相关方面的问题做出正确的判断.

练习册系列答案
相关题目
下列物质的用途中,利用其物理性质的是( )
| A、干冰用作冷冻剂 | B、硫酸用于处理碱性废液 | C、氧气用于气焊 | D、生石灰用作干燥剂 |
以下物质的用途与其化学性质无关的是( )
| A、用二氧化碳灭火 | B、用活性炭吸附异味 | C、用稀盐酸除铁锈 | D、用稀有气体做保护气 |
科学的假设与猜想是科学探究的先导和价值所在.在下列假设(猜想)引导下的探究肯定没有意义的选项是( )
| A、探究二氧化硫和水反应可能有硫酸生成 | B、探究铁制品表面红色的物质可能只是四氧化三铁 | C、探究铁与硫酸的反应产生的气体可能是氧气 | D、探究铜在灼烧时出现的黑色物质可能是炭黑 |
已知FeCl3与CuCl2对H2O2分解都有催化作用,为测定并比较二者的催化效率,需要控制的条件包括:①实验温度;②H2O2的浓度;③催化剂质量;④FeCl3与CuCl2的颗粒大小( )
| A、①② | B、②③ | C、全部 | D、①②④ |
下列是对一些实验操作的设计或描述,其中错误的是( )
| A、有气体参加或生成的化学反应需要在密闭容器中进行才能验证其质量守恒 | B、实验室制备气体选择发生装置时,首先要考虑反应物的状态和反应条件 | C、测定未知溶液的酸碱度时,可以将pH试纸直接伸到待测溶液中 | D、检验久置于空气中的氢氧化钠溶液是否变质,可用氯化钡溶液进行验证 |
下列实验方案中,合理的是( )
| A、分离木炭粉和CuO:在空气中充分灼烧 | B、验证质量守恒定律:比较镁条燃烧前后固体质量 | C、制备Fe(OH)3:向FeCl3溶液中加入NaOH溶液,过滤、洗涤、干燥 | D、除去CO2中的HCl和水蒸气:依次通过过量的NaOH溶液、浓硫酸 |
下列实验方法中可行的是( )
| A、用活性炭软化硬水 | B、用向上排空气法收集氢气 | C、用石蕊溶液鉴别稀盐酸和稀硫酸 | D、用点燃闻气味的方法区别棉线和羊毛线 |