题目内容
环保部门对某工厂的废水进行抽样分析,结果表明废水中含少量硫酸,取一定量废水用溶质质量为4%的氢氧化钠溶液中和(已知废水中的其它成分不与氢氧化钠反应),至pH=7时,消耗氢氧化钠溶液的质量为20g,同时测得反应后溶液质量为69g.请计算该工厂排放的废水中硫酸的质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:由氢氧化钠溶液的质量和质量分数根据氢氧化钠与硫酸反应的化学方程式可以计算出硫酸溶液中硫酸的质量;
反应后的溶液质量去掉氢氧化钠溶液的质量就是硫酸溶液的质量.废水中硫酸的质量分数就是废水中硫酸的质量与硫酸溶液质量之比.
反应后的溶液质量去掉氢氧化钠溶液的质量就是硫酸溶液的质量.废水中硫酸的质量分数就是废水中硫酸的质量与硫酸溶液质量之比.
解答:解:设废水中硫酸的质量为x.
H2SO4+2NaOH=Na2SO4+2H20
98 80
x 20g×4%
=
x=0.98g
废水中硫酸的质量分数为
×100%=2%
答案:该工厂排放的废水中硫酸的质量分数为2%
H2SO4+2NaOH=Na2SO4+2H20
98 80
x 20g×4%
| 98 |
| 80 |
| x |
| 20g×4% |
x=0.98g
废水中硫酸的质量分数为
| 0.98g |
| 69g-20g |
答案:该工厂排放的废水中硫酸的质量分数为2%
点评:本题主要考查有关含杂质物质的化学方程式计算和溶质质量分数的计算,难度较大.

练习册系列答案
相关题目
下列说法正确的是( )
| A、食醋的pH大于7 |
| B、稀硫酸能使酚酞溶液变红 |
| C、硫酸钡与水能形成溶液 |
| D、炒菜用的铁锅锅柄上的塑料是热固性 |
 如图是某试剂瓶标签上的内容.
如图是某试剂瓶标签上的内容.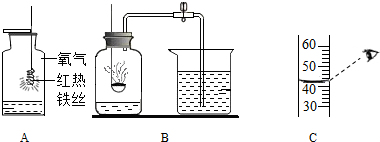


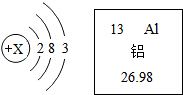 回答下列问题:
回答下列问题: